
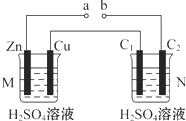
| A. | a、b連接,工作一段時間后裝置M中溶液pH變大,裝置N中溶液pH變小 | |
| B. | a、b連接,裝置M中若有0.1 mol SO42-移到Cu電極,裝置N中C2極放出H2 2.24 L(標準狀況) | |
| C. | a、b未連接時,裝置N中C1電極上有氣體析出 | |
| D. | 不論a、b是否連接,裝置M中觀察到的實驗現象相同 |
分析 如果a、b連接時,左邊裝置是原電池,Zn易失電子作負極、Cu作正極,負極反應式為Zn-2e-=Zn2+、正極反應式為2H++2e-=H2↑,C1是陽極,電極反應式為OH--4e-=2H2O+O2↑,C2是陰極,電極反應式為2H++2e-=H2↑;
如果a、b不連接時,左邊裝置不能構成原電池,只有鋅和稀硫酸發生置換反應,據此分析解答.
解答 解:A.a、b連接,M是原電池,銅電極上氫離子放電生成氫氣,導致溶液酸性減弱,N中電解水,導致硫酸濃度增大,所以工作一段時間后裝置M中溶液pH變大,裝置N中溶液pH變小,故A正確;
B.a、b連接,M是原電池,所以裝置M中若有0.1molSO42-移到Zn電極,而不是銅極,故B錯誤;
C.a、b未連接時,裝置N中不發生反應,所以裝置N中C1電極上無氣體析出,故C錯誤;
D.a、b連接時,裝置M中發生原電池反應,Cu作正極,有氣體生成,a、b不連接時,鋅和氫離子直接反應,接觸面上析出氣體,所以觀察到的實驗現象不相同,故D錯誤;
故選A.
點評 本題考查原電池和電解池原理,明確各個電極上發生的反應是解本題關鍵,知道電解質溶液中陰陽離子移動方向,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 離子半徑:c>b>a | |
| B. | a與c形成化合物的溶液有毒,要密封保存于玻璃瓶中 | |
| C. | a2b2與d的一種較高價態離子的鹽溶液混合時會產生大量的b2 | |
| D. | d高價離子在溶液中與c的低價離子因發生氧化還原反應而不能大量共存 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
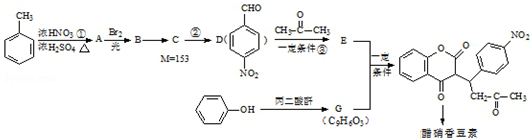
 +H2O
+H2O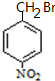 G
G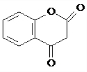
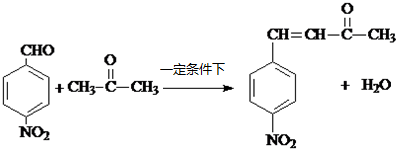
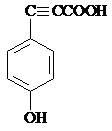 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 氫氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 開始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2[ | 5.4 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含有極性鍵的分子一定是極性分子 | |
| B. | 鍵能越大,表示該分子越容易受熱分解 | |
| C. | 在分子中,兩個成鍵的原子間的距離叫做鍵長 | |
| D. | H-Cl的鍵能為431.8KJ/mol,H-I的鍵能為298.7 KJ/mol,這可以說明HCl比HI分子穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | VSEPR模型就是分子的空間構型 | |
| B. | 在共價化合物分子中一定存在σ鍵 | |
| C. | Na3[AlF6]、Na2[SiF6]和[Cu(NH3)4]Cl2的配位數都是6 | |
| D. | 共價鍵鍵長越短,鍵能一定越大 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com