
某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五種陽離子,現用過量的H2SO4、NaOH、NH3·H2O、NaCl四種溶液,按圖所示步驟分開五種離子。下列判斷正確的是

A.沉淀乙是氫氧化鋁和氫氧化銀的混合物
B.溶液3中含有Al3+
C.試劑①是NaCl,試劑④是H2SO4
D.溶液4含有三種陽離子,分別是H+、Na+、K+
科目:高中化學 來源:2015-2016學年四川省高一下第二次段考化學卷(解析版) 題型:選擇題
已知X+Y=M+N為放熱反應,則下列說法正確的是
A.斷裂X和Y的化學鍵所吸收的能量一定高于形成M和N的化學鍵所放 出的能量
出的能量
B.X和Y的總能量一定高于M和N的總能量
C.Y的能量一定高于N
D.因為該反應為放熱反應,故不必加熱就可發生
查看答案和解析>>
科目:高中化學 來源:2016屆湖北省高三5月模擬三理綜化學試卷(解析版) 題型:填空題
工業上用化學氣相沉積法制備氮化硅,其反應如下:
3SiCl4(g)+2N2(g)+6H2(g)  Si3N4(s)+12HCl(g) ΔH<0
Si3N4(s)+12HCl(g) ΔH<0
某溫度和壓強條件下,分別將1.25mol SiCl4(g)、1.0mol N2(g)、10.5mol H2(g)充入20L密閉容器內,進行上述反應,5min達到平衡狀態,所得Si3N4(s)的質量是35.0g.已知:
化學鍵 | Si-Cl | N≡N | H-H | Si-N | H-Cl |
鍵能(KJ/mol) | a | b | c | d | e |
(1)計算該反應的ΔH=_______________
(2)H2的平均反應速率是
(3)平衡時容器內N2的濃度是
(4)SiCl4(g)的轉化率是 %
(5)下圖為合成Si3N4反應中SiCl4平衡轉化率與溫度、壓強的關系(n(SiCl4)、n(N2)、n(H2)仍按1.25 mol SiCl4(g)、1.0 mol N2(g)、10.5mol H2(g)投入)
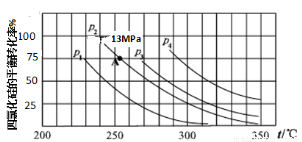
上圖中壓強最大的是_____(P1、P2、P3、P4),列式計算合成Si3N4反應在圖中A點的分壓平衡常數Kp= _______ (用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數,圖中P2=13MPa)
查看答案和解析>>
科目:高中化學 來源:2016屆河北省高三下學期猜題理綜化學試卷(解析版) 題型:選擇題
下列對實驗操作及結論的描述不正確的是
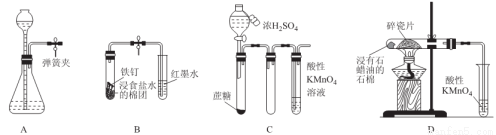
A.夾緊彈簧夾,由漏斗中加水至產生液面差,一段時間后液面差不變,說明氣密性良好
B.打開彈簧夾,紅墨水倒吸入導氣管中,說明鐵釘發生了吸氧腐蝕
C.滴入濃硫酸后,高錳酸鉀溶液褪色,說明濃硫酸使蔗糖脫水的同時還產生了二氧化硫
D.加熱片刻后高錳酸鉀溶液褪色,說明石蠟油分解產生了乙烯
查看答案和解析>>
科目:高中化學 來源:2016屆山東省高三高考打靶測試理綜化學試卷(解析版) 題型:填空題
【化學選修3:物質結構與性質】太陽能電池板材料除單晶硅外,還有銅、銦、鎵、硒、硅等化學物質。
(1)基態銅原子的電子排布式為____________________;已知高溫下CuO Cu2O+O2,從銅原子價電子層結構(3d和4s軌道上應填充的電子數)變化角度來看,能生成Cu2O的原因是_____________;
Cu2O+O2,從銅原子價電子層結構(3d和4s軌道上應填充的電子數)變化角度來看,能生成Cu2O的原因是_____________;
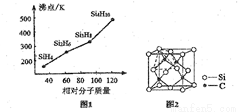
(2)硒、硅均能與氫元素形成氣態氫化物,則它們形成的組成最簡單的氫化物中,分子構型分別為_______、_________,若“Si-H”中共用電子對偏向氫元素,氫氣與硒反應是單質硒是氧化劑,則硒與硅的電負性相對大小為Se_____Si(填“>”、“<”)。人們把硅與氫元素形成的一類化合物叫硅烷,硅烷的組成、結構與相應的烷烴相似,硅烷的沸點與相對分子質量的關系如圖所示,呈現這種變化的原因是_______________;
(3)與鎵元素處于同一主族的硼元素具有缺電子性(價電子數少于價層軌道數),其化合物可與具有孤對電子的分子或離子生成配合物,如BF3能與NH3反應生成BF3·NH3,BF3.NH3中B原子的雜化軌道類型為__________,B與N之間形成________鍵;
(4)金剛砂(SiC)的硬度為9.5,其晶胞結構如圖所示;則金剛砂晶體類型為__________,在SiC中,每個C原子周圍最近的C原子數目為________,若晶胞的邊長為a pm,則金剛砂的密度為__________。
查看答案和解析>>
科目:高中化學 來源:2016屆山東省高三高考打靶測試理綜化學試卷(解析版) 題型:選擇題
用下列分離裝置進行相應實驗,能達到相應實驗目的的是( )

A.用圖I除去CO2中含有的少量Cl2
B.用圖Ⅱ蒸干NH4Cl飽和溶液制備NH4Cl晶體
C.用圖Ⅲ分離NaCl和Na2SO4的混合溶液
D.用圖Ⅳ分離CCl4萃取碘水中的碘后已分層的有機層和水層
查看答案和解析>>
科目:高中化學 來源:2016屆遼寧省高三全真模擬理綜化學試卷(解析版) 題型:填空題
鐵及其化合物有重要用途,如聚合硫酸鐵[Fe2(OH)n(SO4)3n/2]m是一種新型高效的水處理混凝劑,而高鐵酸鉀(其中鐵的化合價為+6)是一種重要的殺菌消毒劑,某課題小組設計如下方案制備上述兩種產品:

請回答下列問題:
(1)若A為H2O(g),寫出反應方程式:_______________________________;
(2)若B為NaClO3與稀硫酸,寫出其氧化Fe2+的離子方程式(還原產物為Cl-)___________________;
(3)若C為KNO3和KOH的混合物,寫出其與Fe2O3加熱共融制得高鐵酸鉀(K2FeO4)的化學方程式,并配平:
□Fe2O3+□KNO3+□KOH □_________+□KNO2+□__________
□_________+□KNO2+□__________
(4)為測定溶液Ⅰ中鐵元素的總含量,實驗操作如下:準確量取20.00mL溶液Ⅰ于帶塞錐形瓶中,加入足量H2O2,調節pH<3,加熱除去過量H2O2;加入過量KI充分反應后,再用0.1000mol?L-1Na2S2O3標準溶液滴定至終點,消耗標準溶液20.00mL.
已知:
2Fe3++2I-═2Fe2++I2
I2+2S2O32-═2I-+S4O42-
①滴定選用的指示劑及滴定終點觀察到的現象_______________________________;
②溶液Ⅰ中鐵元素的總含量為____________g?L-1.若滴定前溶液中H2O2沒有除盡,所測定的鐵元素的含量將_________(填“偏高”“偏低”或“不變”)。
查看答案和解析>>
科目:高中化學 來源:2016屆江西省高三考前熱身理綜化學試卷(解析版) 題型:選擇題
石墨烯可看作將石墨的層狀結構一層一層地剝開得到的單層碳原子;石墨炔是平面網狀結構的全碳分子,具有優良的化學穩定性和半導體性能,還可用于H2的提純;將氫氣氫化到石墨烯排列的六角晶格中,使每個碳原子都增加一個氫原子可得最薄的絕緣新材料石墨烷。下列有關說法中不正確的是
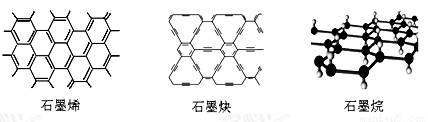
A.石墨烯和石墨炔互為同素異形體
B.石墨炔有望替代二氧化硅用作半導體材料
C.12g石墨烯完全轉變為石墨烷需標況下11.2L氫氣
D.石墨炔孔徑略大于H2分子的直徑,因此它是理想的H2提純薄膜
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省高二6月月考化學試卷(解析版) 題型:選擇題
具有解熱鎮痛及抗生素作用的藥物“芬必得”主要成分的結構簡式為
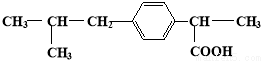 ,它屬于( )
,它屬于( )
①芳香族化合物 ②脂肪族化合物 ③有機羧酸 ④有機高分子化合物 ⑤芳香烴
A、③⑤ B、②③ C、①③ D、①④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com