
對于達到平衡的可逆反應:X+Y W+Z,增大壓強則正、逆反應速率(υ)的變化如圖所示,分析可知X、Y、Z、W的聚集狀態可能是
W+Z,增大壓強則正、逆反應速率(υ)的變化如圖所示,分析可知X、Y、Z、W的聚集狀態可能是
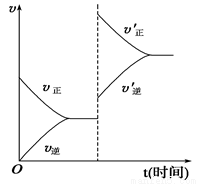
A.Z、W為氣體,X、Y中之一為氣體
B.Z、W中之一為氣體,X、Y為非氣體
C.X、Y、Z皆為氣體,W為非氣體
D.X、Y、Z、W均為氣體
 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源:2016-2017學年湖北宜昌金東方中學、三峽高中高一11月月考化學卷(解析版) 題型:選擇題
如右圖兩集氣瓶體積相等,在同溫、同壓時瓶內氣體的關系一定正確的是
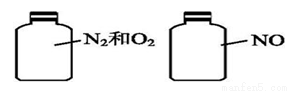
A.所含原子數相等 B.氣體密度相等
C.氣體質量相等 D.摩爾質量相等
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高一上期中化學試卷(解析版) 題型:選擇題
設NA表示阿伏加德羅常數的數值,下列敘述中正確的是( )
A.常溫常壓下,48gO3 和O2混合氣體含有的氧原子數為3NA
B.24g金屬鎂變為鎂離子時失去的電子數為NA
C.4℃時9mL水和標準狀況下11.2L氮氣含有相同的原子數
D.同溫同壓下,NA個NO與NA個N2和O2的混合氣體的體積不相等
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高二上期中化學卷(解析版) 題型:填空題
含氮化合物在生產、生活和科研中有著廣泛的應用。
(1)工業上采用NH3為還原劑處理煙氣(假設煙氣中的NO和NO2的物質的量相等,且反應產物為無毒氣體),測量逸出氣體中氮氧化物含量,從而確定煙氣脫氮率。如圖,下列列說法正確的是(填寫下列字母編號)
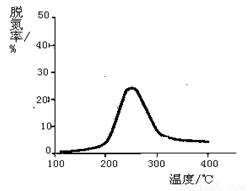
a.相同條件下,改變壓強對脫氮率有影響
b.曲線最高點表示此時平衡轉化率最高
c.相同條件下,加入不同的催化劑能夠改變反應物的轉化率
d.上述反應的化學方程式為:NO+NO2+2NH3 2N2
2N2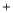 3H2O
3H2O
(2)已知: 2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H=-43.0KJ·mol-1
CO(NH2)2(s)+H2O(g) △H=-43.0KJ·mol-1
—定條件下,將2molNH3和1molCO2充入容積為2L的密閉容器中發生反應。反應進行2min時,放出熱量21.5kJ,則2min內該反應的反應速率υ(NH3)= ,此時混合氣體中NH3的體積分數為 。
(3)在25℃下,將a mol•L-1的NH4NO3溶液與0.01mol•L-1的NaOH等體積混合,反應平衡時,測得溶液pH=7,則NH4NO3溶液的物質的量濃度a___________0.01mol•L-1(填“>”、“<”或“=”);滴加NaOH的過程中水的電離平衡將 (填“正向”、“不”或“逆向”)移動。請你設計實驗,比較NH3 • H2O的電離程度和NH4NO3的水解程度大小 。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高二上期中化學卷(解析版) 題型:選擇題
常溫下,已知Ksp(AgCl)>Ksp( AgBr),現將AgCl與AgBr的飽和溶液等體積混合,再加入足量濃AgNO3溶液,下列有關說法不正確的是:
A.根據Ksp(AgCl)>Ksp( AgBr),可知AgCl的溶解能力比AgBr強
B.加入足量濃AgNO3溶液后,AgCl和AgBr的溶度積Ksp均不變
C.加入足量濃AgNO3溶液后,溶液中只有AgBr沉淀
D.在含有AgBr、AgCl固體的懸濁液中,c (Cl-) >c (Br-)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高二上期中化學卷(解析版) 題型:選擇題
下列事實不能用化學平衡移動原理解釋的是( )






 A.工業合成氨時使用催化劑
A.工業合成氨時使用催化劑
 B.配制SnCl2溶液時加入一定量的鹽酸
B.配制SnCl2溶液時加入一定量的鹽酸
 C.25℃時,在稀硫酸溶液中由水電離出的c(H+)<1×10-7mol/L
C.25℃時,在稀硫酸溶液中由水電離出的c(H+)<1×10-7mol/L
 D.AgCl在水中的溶解度大于在飽和NaCl溶液中的溶解度
D.AgCl在水中的溶解度大于在飽和NaCl溶液中的溶解度
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江佳木斯一中高一上月考二化學卷(解析版) 題型:實驗題
下圖是中學化學中常用于混合物的分離和提純的裝置,請根據裝置回答問題:
(1)寫出圖中標序號的對應儀器名稱:② ,③ 。儀器②中水流方向為 (填“上進下出”或 “下進上出”)
(2)選擇合適的實驗方法分離下列混合物,用代表整套裝置的字母填空;
①從氯化鉀溶液中得到氯化鉀固體,選擇裝置 ;
②分離飽和食鹽水與沙子的混合物,選擇裝置 ;
③除去自來水中的Cl-等雜質以制取蒸餾水,選擇裝置 ;
④分離乙醇和水的混合物,選擇裝置 ;
⑤分離汽油和水的混合物,選擇裝置 ;
(3)分離碘和水的混合物,可選擇下列哪種試劑? (填序號),所得分離方法為 。
A.四氯化碳 B.乙醇 C.蒸餾水
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江佳木斯一中高一上月考二化學卷(解析版) 題型:選擇題
對四組無色透明溶液進行離子檢驗,四位同學各鑒定一組,他們的實驗報告的結論如下,其中可能正確的是
A.Fe3+、K+、I-、Na+ B.Mg2+、NO3-、OH-、Cl-
C.K+、H+、Cl-、CO32- D.Na+、OH-、Cl-、NO3-
查看答案和解析>>
科目:高中化學 來源:2017屆福建省高三上學期第二次月考化學試卷(解析版) 題型:實驗題
有某鐵碳合金,某化學興趣小組為了測定鐵碳合金中鐵的質量分數,并探究濃硫酸的某些性質,設計了下圖所示的實驗裝置和實驗方案(夾持儀器已省略),請你參與此項活動并回答相應問題。

Ⅰ 探究濃硫酸的某些性質
(1)按圖示的 連接裝置,檢查裝置的氣密性,稱量E的質量。
連接裝置,檢查裝置的氣密性,稱量E的質量。
(2)將m g鐵碳合金樣品放入A中,再加入適量的濃硫酸。儀器A的名稱為________。
未點燃酒精燈前,A、B均無明顯現象,其原因是: _。
(3)點燃酒精燈一段時間后,A、B中可觀察到明顯的現象。
寫出A中發生反應的化學方程式_______________________(任寫一個)。B中的現象是______________,由此可得到濃硫酸具有____________性。
(4)隨著反應的進行,A中還可能發生某些離子反應。寫出相應的離子方程式____________(任寫一個)。
(5)反應一段時間后,從A中逸出氣體的速率仍然較快,除因溫度較高,反應放熱外,還可能的原因是______________________。
Ⅱ 測定鐵的質量分數
(6)待A中不再逸出氣體時,停止加熱,拆下E并稱重。E增重b g。
鐵碳合金中鐵的質量分數為_____________________(寫表達式)。
(7)某同學認為上述方法較復雜,使用下圖所示的裝置和其它常用實驗儀器測定某些數據即可。為了快速和準確的計算出鐵的質量分數,最簡便的實驗操作是___________(填寫代號)。
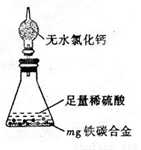
A. 用排水法測定H2的體積
B. 反應 結束后,過濾、洗滌、干燥、稱量殘渣的質量
結束后,過濾、洗滌、干燥、稱量殘渣的質量
C. 測定反應前后裝置和藥品的總質量
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com