
設NA表示阿伏加德羅常數的數值,下列敘述中正確的是( )
A.常溫常壓下,48gO3 和O2混合氣體含有的氧原子數為3NA
B.24g金屬鎂變為鎂離子時失去的電子數為NA
C.4℃時9mL水和標準狀況下11.2L氮氣含有相同的原子數
D.同溫同壓下,NA個NO與NA個N2和O2的混合氣體的體積不相等
科目:高中化學 來源:2016-2017學年山東省菏澤市高一上學期期中化學試卷(解析版) 題型:選擇題
下列溶液中C1﹣的物質的量濃度最大的是( )
A.250 mL 1 mol•L﹣1A1Cl3溶液 B.1000 mL 2.5 mol•L﹣1NaCI溶液
C.200 mL 2 mol•L﹣1MgCl2溶液 D.300 mL 3.5 mol•L﹣1KCl溶液
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高二12月月考化學卷(解析版) 題型:填空題
常溫下,將0.01mol NH4Cl和 0.002mol NaOH 溶于水配成1L 混合溶液。
(1)該溶液中存在的平衡體系有:_________;_________;_________。
(2)溶液中共有____________種不同的微粒。
(3)這些微粒中濃度為0.01mol·L -1的是_________,濃度為0.002mol/L 的是_________。
(4)物質的量之和為0.01mol的三種微粒是:____________。
(5)_________ 、_________ 兩種微粒的物質的量之和比OH-多0.008mol。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高二12月月考化學卷(解析版) 題型:選擇題
化學平衡常數(K)電離常數(Ka、Kb)、溶度積常數(Ksp)等常數是表示、判斷物質性質的重要常數,下列關于這些常數的說法中,正確的是
A.當溫度升高時,弱酸、弱堿的電離常數(Ka、Kb)均變大
B.Ka(HCN)<Ka(CH3COOH)說明相同物質的量濃度時,氫氰酸的酸性比醋酸的強
C.向氯化鋇溶液中加入等體積同濃度的碳酸鈉和硫酸鈉溶液,先產生BaSO4沉淀,則Ksp(BaSO4)>Ksp(BaCO3)
D.化學平衡常數的大小與溫度、濃度、壓強有關,與催化劑無關
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高一上期中化學試卷(解析版) 題型:選擇題
己知在堿性溶液中可發生如下反應:2R(OH)3 + 3C1O- + 4OH- = 2RO4 n-+3Cl- +5H2O。則RO4n-中 r 的化合價是
n-+3Cl- +5H2O。則RO4n-中 r 的化合價是
A.+3 B.+4 C.+5 D.+6
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高一上期中化學試卷(解析版) 題型:選擇題
下列變化中,加入氧化劑可實現的是( )
A.I-→I2 B.Fe3+→Fe2+ C. FeO→Fe  D.HCl→AgCl
D.HCl→AgCl
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高一上期中化學試卷(解析版) 題型:選擇題
下列關于鈉的說法中不正確的是
A.金屬鈉和氧氣反應,條件不同,產物則不同
B.鈉長期放置在空 氣中,最終將變成碳酸鈉
氣中,最終將變成碳酸鈉
C.鈉的化學性質比較活潑,少量的鈉可以保存在與鈉不反應的煤油中
D.將一小塊鈉投入氯化鐵溶液時,既能產生氣體又會出現白色沉淀
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省高二上期中化學卷(解析版) 題型:選擇題
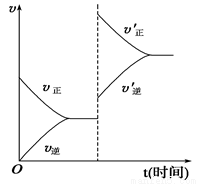
對于達到平衡的可逆反應:X+Y W+Z,增大壓強則正、逆反應速率(υ)的變化如圖所示,分析可知X、Y、Z、W的聚集狀態可能是
W+Z,增大壓強則正、逆反應速率(υ)的變化如圖所示,分析可知X、Y、Z、W的聚集狀態可能是
A.Z、W為氣體,X、Y中之一為氣體
B.Z、W中之一為氣體,X、Y為非氣體
C.X、Y、Z皆為氣體,W為非氣體
D.X、Y、Z、W均為氣體
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省高一12月月考化學卷(解析版) 題型:推斷題
A、B、C、D、E五種物質的焰色反應都呈黃色,A、B分別與水反應都有氣體放出,同時都生成C溶液,A 與水反應放出的氣體具有還原性,B與水反應放出的氣體具有氧化性,C與適量的F氣體反應生成D,D溶液與F氣體反應生成E,E加熱能夠生成D、F氣體和水。根據以上敘述回答下列問題:
與水反應放出的氣體具有還原性,B與水反應放出的氣體具有氧化性,C與適量的F氣體反應生成D,D溶液與F氣體反應生成E,E加熱能夠生成D、F氣體和水。根據以上敘述回答下列問題:
(1)寫出下列物質的化學式:
A__________B__________,C__________,D_________
(2)按要求完成方程式:
①E加熱生成D和F的化學方程式_______________________________;
②C溶液和CO2反應生成D的離子方程式______________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com