

| A. | T1>T2 | B. | 化學方程式系數a>c+d | ||
| C. | 升高溫度,平衡向逆反應方向移動 | D. | 使用催化劑,C的物質的量分數增加 |
分析 可逆反應,當其他條件一定時,溫度越高,反應速率越大,達到平衡所用的時間越短.由圖象(1)可知T2>T1,溫度越高,平衡時C的體積分數φ(C)越小,故此反應的正反應為放熱反應;當其他條件一定時,壓強越高,反應速率越大,達到平衡所用的時間越短.由圖(2)可知p2>p1,壓強越大,平衡時C的體積分數φ(C)越小,可知正反應為氣體物質的量增大的反應,即a<c+d,據此結合外界條件對化學平衡的影響分析解答.
解答 解:可逆反應,當其他條件一定時,溫度越高,反應速率越大,達到平衡所用的時間越短.由圖象(1)可知T2>T1,溫度越高,平衡時C的體積分數φ(C)越小,故此反應的正反應為放熱反應;當其他條件一定時,壓強越高,反應速率越大,達到平衡所用的時間越短.由圖(2)可知p2>p1,壓強越大,平衡時C的體積分數φ(C)越小,可知正反應為氣體物質的量增大的反應,即a<c+d;
A、據上述分析,得到T1<T2,故A錯誤;
B、壓強越大,平衡時C的體積分數φ(C)越小,可知正反應為氣體物質的量增大的反應,即a<c+d,故B錯誤;
C、T2>T1,溫度越高,平衡時C的體積分數φ(C)越小,故此反應的正反應為放熱反應,升溫平衡逆向移動,故C正確;
D、催化劑只改變化學反應速率,對平衡移動沒有影響,C的質量分數不變,故D錯誤;
故C.
點評 本題考查化學平衡圖象問題,題目難度中等,本題注意根據圖象判斷外界條件對平衡的移動的影響是解答該題的關鍵.


科目:高中化學 來源: 題型:解答題
 科學家利用太陽能分解水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇,并開發出直接以甲醇為燃料的燃料電池.已知1mol H2(g)、CO(g)和CH3OH(l)的燃燒放出的熱量為分別為285.8kJ、283.0kJ和726.5kJ.請回答下列問題:
科學家利用太陽能分解水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇,并開發出直接以甲醇為燃料的燃料電池.已知1mol H2(g)、CO(g)和CH3OH(l)的燃燒放出的熱量為分別為285.8kJ、283.0kJ和726.5kJ.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.016 | B. | 1.00 | C. | 0.986 | D. | 2.24 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CaCO3俗名石灰石,屬于碳酸鹽 | |
| B. | CaCO3屬于含氧酸鹽 | |
| C. | 實驗室用煅燒CaCO3來制備二氧化碳 | |
| D. | CaCO3 屬于難溶性的鈣鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在101KPa時,1molCH4完全燃燒生成CO2和水蒸氣放出的熱量就是CH4的燃燒熱 | |
| B. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,則含40.0g NaOH的稀溶液與稀醋酸完全中和,放出大于57.3kJ的熱量 | |
| C. | 己知2C(s)+2O2(g)=2CO2(g)△H=a;2C(s)+O2(g)=2CO(g);△H=b,則a>b | |
| D. | 已知C(石墨,s)=C(金剛石,s)△H>0,則石墨比金剛石穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在標準狀況下,22.4L H2O的分子數為NA | |
| B. | 48g O3氣體含有NA個O3分子 | |
| C. | 0.5mol•L-1 AlCl3溶液中含有0.5NA個Al3+ | |
| D. | 1molMg變為Mg2+時失去的電子數目為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬鋁加到硝酸汞溶液中:2Al+3Hg2+═2Al3++3Hg | |
| B. | 硫酸與氫氧化鋇溶液混合:Ba2++OH-+H++SO${\;}_{4}^{2-}$═BaSO4↓+H2O | |
| C. | 飽和石灰水跟稀硝酸反應:Ca(OH)2+2H+═Ca2++2H2O | |
| D. | 碳酸鈣溶于醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 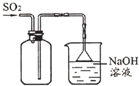 收集SO2 收集SO2 | |
| B. | 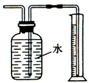 測量Cu與濃硝酸反應生成二氧化氮體積 測量Cu與濃硝酸反應生成二氧化氮體積 | |
| C. | 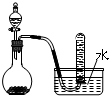 二氧化錳固體和雙氧水制取O2 二氧化錳固體和雙氧水制取O2 | |
| D. | 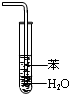 吸收HCl 吸收HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com