
| A. | 1 L 1mol/L NaHCO3溶液中自由移動的離子總數為3NA | |
| B. | 常溫常壓下,1.06g Na2CO3含有Na+數目為0.02NA | |
| C. | 1 mol Na2O2與CO2反應電子轉移為2 NA | |
| D. | 40g NaOH溶解在1 L水中,得到溶液的物質的量濃度為1 mol/L |
分析 A、求出碳酸氫鈉的物質的量,然后根據1mol碳酸氫鈉只能完全電離為鈉離子和碳酸氫根來分析;
B、求出碳酸鈉的物質的量,然后根據1mol碳酸鈉中含2mol鈉離子來分析;
C、過氧化鈉與二氧化碳的反應為歧化反應;
D、將氫氧化鈉溶于1L水中后,溶于體積大于1L.
解答 解:A、溶于中碳酸氫鈉的物質的量n=CV=1mol/L×1L=1mol,而1mol碳酸氫鈉只能完全電離為鈉離子和碳酸氫根,而碳酸氫根的電離程度很小,故溶于溶液中的離子的個數小于3NA個,故A錯誤;
B、1.06g碳酸鈉的物質的量為0.01mol,而1mol碳酸鈉中含2mol鈉離子,故0.01mol碳酸鈉中含0.02mol鈉離子即0.02NA個,故B正確;
C、過氧化鈉與二氧化碳的反應為歧化反應,1mol過氧化鈉轉移1mol電子即NA個,故C錯誤;
D、將氫氧化鈉溶于1L水中后,溶于體積大于1L,則溶液的物質的量濃度小于1mol/L,故D錯誤.
故選B.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 膠體的分散質能透過濾紙 | |
| B. | 膠體能產生丁達爾現象 | |
| C. | 膠體粒子直徑在10-9~10-7 m之間 | |
| D. | 膠體是純凈物,其它分散系是混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
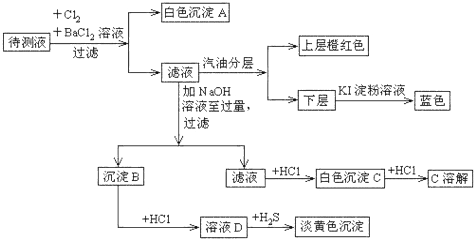
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol/L的NaOH溶液與0.1 mol/L的CH3COOH溶液等體積混合c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| B. | 常溫下,0.01 mol/L的NaOH溶液與pH=2的CH3COOH溶液等體積混合c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 常溫下,0.1 mol/L的CH3COOH溶液與0.1 mol/L的NaOH溶液混合后使pH=7,c(CH3COO-)═c(Na+)>c(H+)=c(OH-) | |
| D. | 0.1 mol/L的CH3COOH溶液和0.1 mol/L的CH3COONa溶液等體積混合c(CH3COO-)+c(OH-)═c(Na+)+c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 每消耗1 mol C3H8可以向外電路提供12 mol e- | |
| B. | 負極通入C3H8,發生還原反應 | |
| C. | 正極通入氧氣和CO2,正極反應式是:O2+2CO2+4e-═2CO32- | |
| D. | CO32-移向電池的正極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原混合溶液中c(Na+)=0.2 mol•L-1 | |
| B. | 電解后溶液中c(H+)=0.4mol•L-1 | |
| C. | 上述電解過程中共轉移0.4 mol電子 | |
| D. | 電解后得到的Cu的物質的量為0.05mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷、甲醛、甲酸都不存在同分異構體,則甲醚(CH3OCH3)也無同分異構體 | |
| B. | 淀粉、油脂、蛋白質、纖維素都能在人體內水解,也能在體內氧化提供能量 | |
| C. | 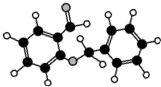 如圖所示的有機物分子式為C14H12O2,能發生銀鏡反應 | |
| D. | 在堿性條件下,CH3CO18OC2H5的水解產物是CH3COOH和C2H518OH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在pH=12的溶液中:K+、Cl-、HCO3-、Na+ | |
| B. | 在[H+]=10-12 mol•L-1的溶液:K+、Ba2+、Cl-、Br- | |
| C. | 使酚酞試液變紅的溶液:Na+、Cl-、SO42-、Fe3+ | |
| D. | 使石蕊試液變紅的溶液:K+、MnO4-、I-、H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com