
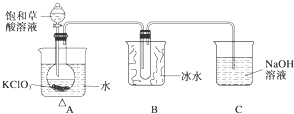
 某研究性學習小組組裝了下圖所示的裝置制備ClO2氣體(加熱裝置用“△”表示),反應原理為飽和草酸溶液與KClO3粉末在60℃時反應制得ClO2(溫度過高或過低都會影響制氣效率).
某研究性學習小組組裝了下圖所示的裝置制備ClO2氣體(加熱裝置用“△”表示),反應原理為飽和草酸溶液與KClO3粉末在60℃時反應制得ClO2(溫度過高或過低都會影響制氣效率).| 實驗步驟 | 預期現象和結論 |
| 步驟1:取少量沉淀于試管中,加入足量0.1 mol•L-1 HCl. | |
| 步驟2:往步驟1的剩余物中,再滴加幾滴0.01 mol•L-1 KMnO4. |
分析 (1)根據質量守恒和得失電子守恒配平方程式;
(2)反應原理為飽和草酸溶液與KClO3粉末在60℃時反應制得ClO2分析,ClO2沸點較低,易液化;
(3)草酸可與生成物碳酸氫鉀反應生成二氧化碳,或KClO3氧化草酸生成二氧化碳氣體;
(4)①沉淀可能為CaCO3或CaC2O4或二者都有;
②利用鹽酸和碳酸鈣反應生成二氧化碳氣體能使澄清石灰水變渾濁驗證碳酸鈣的存在,加入的酸溶解生成的草酸和高錳酸鉀溶液反應使溶液褪色來設計實驗進行驗證草酸鈣的存在.
解答 解:(1)由質量守恒和得失電子守恒可配平,方程式為2KClO3+H2C2O4=2KHCO3+2ClO2↑,故答案為:2;1;2;2;
(2)反應原理為飽和草酸溶液與KClO3粉末在60℃時反應制得ClO2,需要溫度計控制溫度,A裝置中還缺少的一樣儀器名稱是為溫度計,ClO2的沸點較低,易液化,B可起到冷凝收集的作用,
故答案為:溫度計;將ClO2冷凝收集;
(3)反應后生成KHCO3,過量的草酸與KHCO3反應:HOOC-COOH+KHCO3=CO2↑+H2O+HOOC-COOK,逸出的CO2與NaOH溶液反應生成Na2CO3,CO2+2NaOH=Na2CO3+H2O,
也可能為因KClO3具有較強氧化性,將草酸氧化成CO2,逸出的CO2與NaOH溶液反應生成Na2CO3,
故答案為:過量的草酸與KHCO3反應:HOOC-COOH+KHCO3=CO2↑+H2O+HOOC-COOK,逸出的CO2與NaOH溶液反應生成Na2CO3,CO2+2NaOH=Na2CO3+H2O;或因KClO3具有較強氧化性,將草酸氧化成CO2,逸出的CO2與NaOH溶液反應生成Na2CO3;
(4)①沉淀可能為CaCO3或CaC2O4或二者都有,故答案為:只存在CaC2O4;
②進行實驗先檢驗碳酸鈣的存在,再利用加入的酸溶解生成的草酸和高錳酸鉀溶液反應使溶液褪色來設計實驗進行驗證,取少量沉淀于試管中,加入足量1 mol•L-1 HCl,將產生的氣體通入澄清石灰水中,澄清石灰水變渾濁,說明菠菜中含有碳酸鹽,向步驟1得到的溶液中滴加幾滴0.01 mol•L-1 KMnO4溶液紫紅色褪去,說明菠菜中含有草酸鹽,
故答案為:
| 實驗步驟 | 預期現象和結論 |
| 足量0.1 mol•L-1 HCl | 沉淀全部溶解,有氣泡產生,說明沉淀中有CaCO3 |
| 往步驟1的剩余物中,再滴加幾滴0.01 mol•L-1 KMnO4 | 溶液紫紅色褪去,說明沉淀中有CaC2O4,結合步驟1,假設2成立 |
點評 本題考查了物質性質的實驗設計和實驗分析判斷,側重于學生的分析能力和實驗能力的考查,為高考常見題型和高頻考點,掌握實驗基礎和物質性質是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:實驗題
 三草酸合鐵酸鉀晶體(K3[Fe(C2O4)3]•xH2O)是一種光敏材料,110℃時失去全部結晶水.某實驗小組為測定該晶體中鐵的含量,做了如下實驗,完成下列填空:
三草酸合鐵酸鉀晶體(K3[Fe(C2O4)3]•xH2O)是一種光敏材料,110℃時失去全部結晶水.某實驗小組為測定該晶體中鐵的含量,做了如下實驗,完成下列填空:| 滴定次數 | 滴定起始讀數(mL) | 滴定終點讀數(mL) |
| 第一次 | 1.08 | 如圖 |
| 第二次 | 2.02 | 24.52 |
| 第三次 | 1.00 | 20.98 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
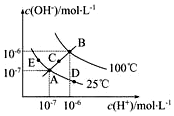 已知水的電離平衡曲線如圖示,試回答下列問題:
已知水的電離平衡曲線如圖示,試回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 熱穩定性:HBr<HCl<HF | B. | 原子半徑:I<Br<Cl | ||
| C. | 酸性:HClO4<HBrO4<HIO4 | D. | 非金屬性:F<Cl<Br |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 ,B原子L層的電子總數是K層的3倍;0.1mol C單質能從酸中置換出2.24L氫氣(標準狀況),同時它的電子層結構變得與氖原子的電子層結構相同;D離子的半徑比C離子的小,D離子與B離子的電子層結構相同.
,B原子L層的電子總數是K層的3倍;0.1mol C單質能從酸中置換出2.24L氫氣(標準狀況),同時它的電子層結構變得與氖原子的電子層結構相同;D離子的半徑比C離子的小,D離子與B離子的電子層結構相同.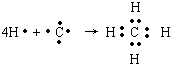 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
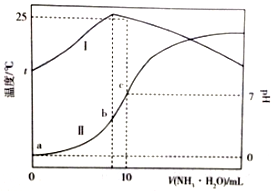 溫度為t℃時,在10mL1.0mol/L的鹽酸中,逐滴滴入xmol/L的氨水,隨著氨水遂漸加入,溶液中的溫度變化曲線(曲線I)和pH變化曲線(曲線II)如圖所示(忽略混合時溶液體積的變化).下列有關判斷正確的是( )
溫度為t℃時,在10mL1.0mol/L的鹽酸中,逐滴滴入xmol/L的氨水,隨著氨水遂漸加入,溶液中的溫度變化曲線(曲線I)和pH變化曲線(曲線II)如圖所示(忽略混合時溶液體積的變化).下列有關判斷正確的是( )| A. | c點時,c(NH3•H2O)=1.0mol•L-1 | B. | a點時,水的電離程度最大 | ||
| C. | b點時,c(NH4+)>c(Cl-)>c(H+)>c(OH-) | D. | c點時,c(NH3•H2O)=$\frac{x-1}{2}$mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{vn}{22.4}$ | B. | $\frac{22.4n}{v}$ | C. | $\frac{vn}{5.6}$ | D. | $\frac{22.4n}{3v}$ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com