
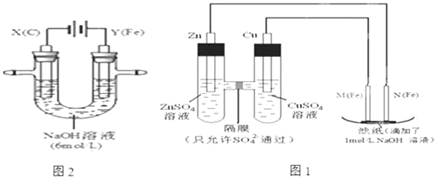
���� ��D1�У���߅�b����ԭ늳أ��^��Ľ����\��ؓ�O���^����Ľ����~�����O�����Ҫ��늘O���ϴ����~�����Ҳ��ϱ���Dz����\��Ľ��ٻ�?q��)�늵ķǽ��٣�M��ꖘO��N��ꎘO��늽����ꎘO����x�ӵ���Ӱl(f��)��߀ԭ������ԭ늳ط�늕r����x����ؓ�O�Ƅӣ�
��ԓ늽���У�ꖘO�����ǻ���٣��t늽�ع����r��ꖘO���Fʧ��Ӱl(f��)������������ͬ�r�������x��ʧ����������⣬ꎘO�Ϛ��x�ӵ���Ӱl(f��)��߀ԭ����������(j��)�ꖘO���D(zhu��n)����Ӕ�(sh��)���Ӌ���F�������|(zh��)�����ډA���\늳��У����O�ϵ���Ӱl(f��)��߀ԭ������
��� �⣺��1���ڱ��C늘O������׃����r�£���Ȼ���\��ؓ�O���t���O���ϱ���Dz����\��Ľ��ٻ�?q��)�늵ķǽ��٣��X�DZ��\��Ľ��٣����Բ��ܴ����~��
�ʴ𰸞飺A��
��2��N늘O�B��ԭ늳�ؓ�O��������늽��ꎘO��ꎘO�Ϛ��x�ӵ���Ӱl(f��)��߀ԭ������늘O����ʽ�飺2H++2e-�TH2������2H2O+2e-�TH2��+2OH-����
�ʴ𰸞飺2H++2e-�TH2������2H2O+2e-�TH2��+2OH-����
��3��ԭ늳ط�늕r����x����ؓ�O�Ƅӣ�������������������Ƅӣ�늽���У�ꎘO�Ϛ��x�ӵ�������ɚ�⣬ꖘO���Fʧ������Ɂ��F�x�ӣ����F�x�Ӻ͚������x�ӷ������ɚ��������F�����������F�������������ɚ������F�����ԞV�����мt��ɫ���c�a(ch��n)����
�ʴ𰸞飺�������� �V�����мt��ɫ���c�a(ch��n)����
��4��늽��^���У�ꎘO�Ϛ��x�ӷ�����ɚ�⣬�tꎘO�����������x�ӝ�ȴ��ښ��x����Һ����Һ�ʉA�ԣ���Һ��pH���ʴ𰸞飺����
��5���F�ǻ���٣�늽�ع����r��ꖘO���Fʧ��Ӱl(f��)�������������������x��ʧ��Ӱl(f��)���������������l(f��)����늘O����ʽ�飺Fe-6e-+8OH-�TFeO42-+4H2O��4OH--4e-�T2H2O+O2�����ʴ𰸞飺4OH--4e-�T2H2O+O2����
��6�����O�ϸ��F����x�ӵ���Ӱl(f��)��߀ԭ��������������ʽ��2FeO42-+6e-+5H2O�TFe2O3+10OH-���ʴ𰸞飺2FeO42-+6e-+5H2O�TFe2O3+10OH-��
�c�u ���}������ԭ늳غ�늽��ԭ��������l���c����(c��)���ڌW���ķ��������Ŀ��飬ע��늽��������������ꖘO���t늽�ع����rꖘO����ʧ��Ӱl(f��)�����������������e�c���y���еȣ�


 ȫ��(y��u)�����Ԫ�z�y�����w�����ϵ�д�
ȫ��(y��u)�����Ԫ�z�y�����w�����ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
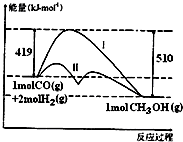 ���ڷ���CO��g��+2H2��g��?CH3OH��g����H�������^���е�����׃����r��D��ʾ������I������II�քe��ʾ��ʹ�ô�����ʹ�ô����ăɷN��r�������Д����_���ǣ�������
���ڷ���CO��g��+2H2��g��?CH3OH��g����H�������^���е�����׃����r��D��ʾ������I������II�քe��ʾ��ʹ�ô�����ʹ�ô����ăɷN��r�������Д����_���ǣ�������| A�� | ԓ�����ġ�H=+91kJ/mol | |
| B�� | ���������ԓ�����ġ�H׃С | |
| C�� | ������Ŀ���������������Ŀ����� | |
| D�� | ���ԓ��������Һ�B(t��i)CH3OH�r���H1���t��H1����H |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | HCl | B�� | NH4Cl | C�� | CH3COONa | D�� | NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
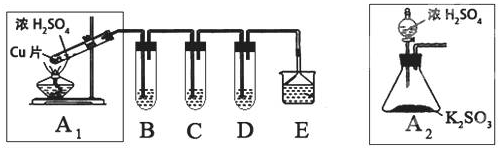
| ������ | �A�ڬF(xi��n)���c�Y(ji��)Փ |
| ���E1��ȡ�m��������Һ����С�����У����z�^�ι�ȡ1mol/L BaCl2��Һ��С�����μ�ֱ���^���� | �����F(xi��n)��ɫ���ᣬ�t��Һ�д���SO32-�� SO42-�� |
| ���E2����С�����еĝ�Һ�^�V��ϴ�죬�����m��ˮ�Ѹ��ڞV���ϵĹ��w�_����һС�����У���_�µĹ��w����1�Σ���������Ʒ�t���ٵ����^��2mol/L�}�ᣬ��ʎ�� | |
| ���E3����ԇ��ȡ�m���VҺ�������У���С�����У������^����1mol/LBa��OH��2��Һ[�����1�Σ���������Ʒ�t��Һ���ٵ���2-3�Σ����^������2mol/L�}��]����ʎ |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | FeO | B�� | Fe2O3 | C�� | Fe3O4 | D�� | �o���_�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | ��ɫ������CuI2����ɫ��Һ����I2 | |
| B�� | �μ�KI��Һ�r���D(zhu��n)��1mol��ӕr����1mol��ɫ���� | |
| C�� | ͨ��SO2�r��SO2�cI2������I2��߀ԭ�� | |
| D�� | �������l���£����|(zh��)�������ԣ�I2��Cu2+��SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| �x� | ���������F(xi��n)�� | ���Y(ji��)Փ |
| A | ��ij��Һ�м����Ȼ��^��Һ���а�ɫ�������ɣ��ټ��}���ữ���������ܽ� | ԓ��Һ��һ������SO42- |
| B | �Ý����IJ����������Na2O2��Ó֬���⣬Ó֬��ȼ�� | CO2��H2O�cNa2O2�����Ƿşᷴ�� |
| C | ��ij��Һ�м���ϡ�}�ᣬ�a(ch��n)����ʹ����ʯ��ˮ׃����ğoɫ�oζ���w | ԓ��Һ��һ������CO32- |
| D | ���K�zպȡij��Һ�ڟoɫ�������Ɵ�ֱ���^������ɫδҊ��ɫ | ԭ��Һ�в���K+ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | ������OH-����Һ��Ba2+��K+��NO3-��AlO2- | |
| B�� | ����Na2O2��ĩ����Һ��Na+��Cl-��SO32-��OH- | |
| C�� | c��KNO3��=1.0mol/L����Һ��H+��I-��Cl-��Ca2+ | |
| D�� | ������ɫʯ��ԇҺ���{ɫ����Һ��Fe3+��Ba2+��HCO3-��Br- |
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com