
一定條件下,將一定量的A、B、C、D四種物質(zhì),置于密閉容器中發(fā)生如下反應(yīng):
m A(s)+n
B(g)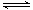 p
C(g)+q D(g) △H 達(dá)到平衡后,測(cè)得B的濃度為0.5
mol/L。保持溫度不變,將密閉容器的容積擴(kuò)大到原來的兩倍,再次達(dá)到平衡后,測(cè)得B的濃度為0.3mol·L-1。當(dāng)其它條件不變時(shí),C在反應(yīng)混合物中的體積分?jǐn)?shù)(
p
C(g)+q D(g) △H 達(dá)到平衡后,測(cè)得B的濃度為0.5
mol/L。保持溫度不變,將密閉容器的容積擴(kuò)大到原來的兩倍,再次達(dá)到平衡后,測(cè)得B的濃度為0.3mol·L-1。當(dāng)其它條件不變時(shí),C在反應(yīng)混合物中的體積分?jǐn)?shù)(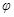 )與溫度(T)、時(shí)間(t)的關(guān)系如圖所示。下列敘述正確的是
)與溫度(T)、時(shí)間(t)的關(guān)系如圖所示。下列敘述正確的是

A.熱化學(xué)方程式中:n<p+q
B.熱化學(xué)方程式中:△H>0
C.達(dá)平衡后,增加A的量,有利于提高B的轉(zhuǎn)化率
D.若T1、T2時(shí)反應(yīng)的平衡常數(shù)分別為K1、K2,則K1>K2
D
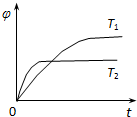
【解析】密閉容器的容積擴(kuò)大到原來的兩倍的瞬間,B的濃度應(yīng)是0.25mol/L,但最終平衡時(shí)B的濃度為0.3mol·L-1,這說明降低壓強(qiáng),平衡向逆反應(yīng)方向進(jìn)行,即正反應(yīng)是體積減小的反應(yīng),所以n>p+q,A不正確。根據(jù)圖像可知,溫度為T2的曲線首先達(dá)到平衡狀態(tài),即T2大于T1。溫度越高,C的體積分?jǐn)?shù)越小,石墨升高溫度平衡向逆反應(yīng)方向進(jìn)行,即正反應(yīng)是放熱反應(yīng),B不正確。A是固體,不影響平衡狀態(tài),C不正確。升高溫度平衡向逆反應(yīng)方向進(jìn)行,所以平衡常數(shù)減小,D正確,答案選D。



| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
 (2011?崇文區(qū)模擬)一定條件下,將一定量的A、B、C、D四種物質(zhì),置于密閉容器中發(fā)生如下反應(yīng):
(2011?崇文區(qū)模擬)一定條件下,將一定量的A、B、C、D四種物質(zhì),置于密閉容器中發(fā)生如下反應(yīng): p C(g)+q D(g)達(dá)到平衡后,測(cè)得B的濃度為0.5
p C(g)+q D(g)達(dá)到平衡后,測(cè)得B的濃度為0.5查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
 一定條件下,將一定量的A、B、C、D四種物質(zhì),置于密閉容器中發(fā)生如下反應(yīng):
一定條件下,將一定量的A、B、C、D四種物質(zhì),置于密閉容器中發(fā)生如下反應(yīng):| A、熱化學(xué)方程式中:n<p+q | B、熱化學(xué)方程式中:△H>0 | C、達(dá)平衡后,增加A的量,有利于提高B的轉(zhuǎn)化率 | D、若T1、T2時(shí)反應(yīng)的平衡常數(shù)分別為K1、K2,則K1>K2 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
現(xiàn)將N2和H2在一定條件下合成氨。
(1)有一體積比為2∶3的N2和H2的混合氣體,在一體積不變的密閉容器中發(fā)生反應(yīng),達(dá)到平衡時(shí),容器內(nèi)的壓強(qiáng)為反應(yīng)開始時(shí)的4/5,求:
①N2的轉(zhuǎn)化率?
②平衡時(shí)n(N2)、n(H2)和n(NH3)的體積比是多少?
(2)在一定條件下,將一定量的N2和H2混合氣體合成氨,達(dá)平衡時(shí),混合氣體中NH3的體積分?jǐn)?shù)為25%。若反應(yīng)前后條件相同,則反應(yīng)從開始到平衡縮小的氣體體積與原反應(yīng)物氣體體積的比值是多少?
查看答案和解析>>
科目:高中化學(xué) 來源:2012-2013學(xué)年山東省濟(jì)寧市魚臺(tái)一中高二3月月考化學(xué)試卷(帶解析) 題型:單選題
一定條件下,將一定量的A、B、C、D四種物質(zhì),置于密閉容器中發(fā)生如下反應(yīng):
m A(s)+n B(g) p C(g)+q D(g) △H
p C(g)+q D(g) △H
達(dá)到平衡后,測(cè)得B的濃度為0.5 mol/L。保持溫度不變,將密閉容器的容積擴(kuò)大到原來的兩倍,再次達(dá)到平衡后,測(cè)得B的濃度為0.3mol·L-1。當(dāng)其它條件不變時(shí),C在反應(yīng)混合物中的體積分?jǐn)?shù)( )與溫度(T)、時(shí)間(t)的關(guān)系如下圖所示。下列敘述正確的是( )
)與溫度(T)、時(shí)間(t)的關(guān)系如下圖所示。下列敘述正確的是( )
A.熱化學(xué)方程式中:n<p+q
B.熱化學(xué)方程式中:△H>0
C.達(dá)平衡后,增加A的量,有利于提高B的轉(zhuǎn)化率
D.若T1、T2時(shí)反應(yīng)的平衡常數(shù)分別為K1、K2,則K1>K2
查看答案和解析>>
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com