
【題目】納米級Cu2O由于具有優良的催化性能而受到關注,下表為制取Cu2O的兩種方法:
方法a | 用炭粉在高溫條件下還原CuO |
方法b | 電解法,反應為2Cu+H2O |
(1)工業上常用方法b制取Cu2O而很少用方法a,其原因是反應條件不易控制,若控溫不當易生成__________而使Cu2O產率降低。
(2)已知:①2Cu(s)+ ![]() O2(g)=Cu2O(s) ΔH1=-169 kJ·mol-1
O2(g)=Cu2O(s) ΔH1=-169 kJ·mol-1
②C(s)+ ![]() O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
③Cu(s)+ ![]() O2(g)=CuO(s) ΔH3=-157 kJ·mol-1
O2(g)=CuO(s) ΔH3=-157 kJ·mol-1
則方法a中發生的反應:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=________。
(3)方法b是用肼燃料電池為電源,通過離子交換膜電解法控制電解液中OH-的濃度來制備納米Cu2O,裝置如圖所示:
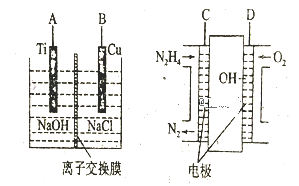
①上述裝置中B電極應連_________電極(填“C”或“D”)。
②該離子交換膜為____離子交換膜(填“陰”或“陽”),該電解池的陽極反應式為_______。
③原電池中負極反應式為______________。
【答案】Cu +34.5kJ·mol-1 D 陰 2Cu-2e-+2OH-=Cu2O+H2O N2H4-4e-+4OH-=N2↑+4H2O
【解析】
(1)碳會將CuO還原為銅;
(2)根據蓋斯定律進行求解;
(3)①銅電極應發生氧化反應;原電池中正極得電子發生還原反應,負極失電子發生氧化反應;
②離子交換膜要控制電解液中OH-的濃度,陰離子交換膜才能控制氫氧根濃度;
③原電池中負極失電子發生氧化反應。
(1)在加熱條件下,C會將CuO還原為Cu,故方法I反應條件不易控制,若控溫不當易生成Cu而使Cu2O產率降低;
(2)已知:①2Cu(s)+![]() O2(g)=Cu2O(s)△H=-169kJmol-1
O2(g)=Cu2O(s)△H=-169kJmol-1
②C(s)+![]() O2(g)=CO(g)△H=-110.5kJmol-1
O2(g)=CO(g)△H=-110.5kJmol-1
③Cu(s)+![]() O2(g)=CuO(s)△H=-157kJmol-1
O2(g)=CuO(s)△H=-157kJmol-1
根據蓋斯定律①+②-2×2可得2CuO(s)+C(s)=Cu2O(s)+CO(g)△H=+34.5kJmol-1;
(3)①原電池中D電極通入氧氣,氧氣發生還原反應,故D電極為正極,C電極為負極;電解池中B電極為銅,銅在反應過程被氧化,故為陽極,與外接電源的正極相連,即與D相連,故答案為:D;
②該方法采用離子交換膜控制電解液中OH-的濃度,則只有使用陰離子交換膜才能控制氫氧根離子濃度;在電解池中,當陽極是活潑電極時,該電極本身發生失電子得還原反應,在堿性環境下,金屬銅失去電子的電極反應為2Cu-2e-+2OH-=Cu2O+H2O;
③原電池中負極失電子發生氧化反應,負極通入N2H4失電子被氧化成N2,負極反應式為N2H4-4e-+4OH-=N2↑+4H2O。


科目:高中化學 來源: 題型:
【題目】下列有關試劑的保存方法, 錯誤的是
A.氫氟酸盛裝在細口玻璃瓶中
B.氫氧化鈉溶液裝在用橡膠塞的試劑瓶中
C.硫酸亞鐵溶液存放在加有少量鐵粉的試劑瓶中
D.金屬鈉保存在煤油中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在體積為1 L的密閉容器中(體積不變)充入1mol CO2和3mol H2,一定條件下發生反應:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。下列說法正確的是
CH3OH(g)+H2O(g)。測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。下列說法正確的是
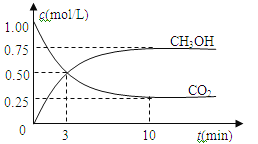
A.進行到3分鐘時,正反應速率和逆反應速率相等
B.10分鐘后容器中各物質濃度不再改變
C.達到平衡后,升高溫度,正反應速率增大、逆反應速率減小
D.3min前v正>v逆,3min后v正<v逆
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向一定量的Cu、Fe2O3的混合物中加入400 mL 1 mol·L-1的鹽酸,恰好使混合物完全溶解,所得溶液中不含Fe3+。若用過量的CO在高溫下還原相同質量的原混合物,固體減少的質量為
A. 2.4 g B. 3.2 g C. 4.8 g D. 6.4 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由硫鐵礦燒渣(主要成分:Fe3O4、Fe2O3和FeO)得到綠礬(FeSO4·7H2O),再通過綠礬制備鐵黃[FeO(OH)]的流程如下:
![]()
已知:FeS2和鐵黃均難溶于水。下列說法錯誤的是( )
A.步驟①后可依次用KSCN溶液和酸性KMnO4溶液來檢測溶液中鐵元素的價態
B.步驟②發生后,溶液的酸性增強
C.步驟③,將溶液蒸發濃縮、冷卻結晶、過濾、洗滌、低溫干燥可得到綠礬
D.為確保鐵黃的產率,盡可能將步驟④中的pH值調大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對可逆反應4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列敘述正確的是( )
4NO(g)+6H2O(g),下列敘述正確的是( )
A. 達到化學平衡時4v正(O2)=5v逆(NO)
B. 若單位時間內生成x mol NO的同時,消耗x mol NH3,則反應達到平衡狀態
C. 達到化學平衡時,若增大容器容積,則正反應速率減小,逆反應速率增大
D. 化學反應速率關系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.一定條件下,在體積為5 L的密閉容器中,A、B、C三種氣體的物質的量n(mol)隨時間t(min)的變化如圖1所示。已知達平衡后,降低溫度,A的體積分數將減小。
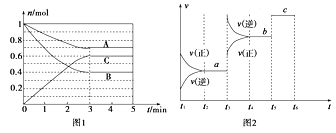
(1)該反應的化學方程式為____________________________。
(2)該反應的反應速率v隨時間t的關系如上圖2所示:
①根據上圖判斷,在t3時刻改變的外界條件是______________。
②a、b、c三點中,C的體積分數最大的是________。
③各階段的平衡常數如下表所示:
t2~t3 | t4~t5 | t5~t6 |
K1 | K2 | K3 |
K1、K2、K3之間的大小關系為________(用“>”、“<”或“=”連接)。
Ⅱ.在密閉容器中充入一定量的H2S,發生反應2H2S(g) ![]() 2H2(g)+S2(g) ΔH,如圖所示為H2S氣體分解生成H2(g)和S2(g)的平衡轉化率與溫度、壓強的關系。
2H2(g)+S2(g) ΔH,如圖所示為H2S氣體分解生成H2(g)和S2(g)的平衡轉化率與溫度、壓強的關系。
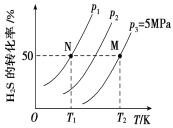
(1)△H_________ (填“>”“<”或“ = ”)0。
(2)圖中壓強(p1、p2、p3)的大小順序為________________。
(3)圖中M點的平衡常數Kp =_______MPa(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)
(4)如果想進一步提高H2S的轉化率,除改變溫度、壓強外,還可以采取的措施有___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醋酸溶液中存在電離平衡:CH3COOH![]() H++CH3COO,下列敘述不正確的是
H++CH3COO,下列敘述不正確的是
A.升高溫度,平衡正向移動,醋酸的電離常數Ka增大
B.0.10 mol/L的CH3COOH溶液加水稀釋,溶液中c(OH-)增大。
C.CH3COOH溶液中加少量的CH3COONa固體,平衡逆向移動
D.25℃時,欲使醋酸溶液的pH、電離常數Ka和電離程度都減小,可加入少量冰醋酸。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器中加入CaSO4和CO,在一定溫度下,發生反應:CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g) ΔH=+218.4 kJ·mol-1
CaO(s)+SO2(g)+CO2(g) ΔH=+218.4 kJ·mol-1

CO的反應速率隨時間變化如圖所示。下列說法正確的是( )
A.該反應是吸熱反應,升高溫度,正反應速率增大,逆反應速率減小
B.CaO是固態,不能用CaO表示反應的快慢
C.圖示中t1時改變的條件可能是減小c(CO),同時增大c(SO2)
D.圖示中t1時改變的條件可能是增大壓強
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com