
【題目】Ⅰ.一定條件下,在體積為5 L的密閉容器中,A、B、C三種氣體的物質(zhì)的量n(mol)隨時間t(min)的變化如圖1所示。已知達(dá)平衡后,降低溫度,A的體積分?jǐn)?shù)將減小。
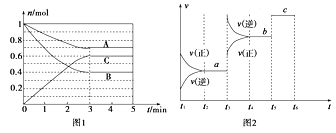
(1)該反應(yīng)的化學(xué)方程式為____________________________。
(2)該反應(yīng)的反應(yīng)速率v隨時間t的關(guān)系如上圖2所示:
①根據(jù)上圖判斷,在t3時刻改變的外界條件是______________。
②a、b、c三點(diǎn)中,C的體積分?jǐn)?shù)最大的是________。
③各階段的平衡常數(shù)如下表所示:
t2~t3 | t4~t5 | t5~t6 |
K1 | K2 | K3 |
K1、K2、K3之間的大小關(guān)系為________(用“>”、“<”或“=”連接)。
Ⅱ.在密閉容器中充入一定量的H2S,發(fā)生反應(yīng)2H2S(g) ![]() 2H2(g)+S2(g) ΔH,如圖所示為H2S氣體分解生成H2(g)和S2(g)的平衡轉(zhuǎn)化率與溫度、壓強(qiáng)的關(guān)系。
2H2(g)+S2(g) ΔH,如圖所示為H2S氣體分解生成H2(g)和S2(g)的平衡轉(zhuǎn)化率與溫度、壓強(qiáng)的關(guān)系。
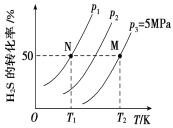
(1)△H_________ (填“>”“<”或“ = ”)0。
(2)圖中壓強(qiáng)(p1、p2、p3)的大小順序?yàn)?/span>________________。
(3)圖中M點(diǎn)的平衡常數(shù)Kp =_______MPa(用平衡分壓代替平衡濃度計(jì)算,分壓=總壓×物質(zhì)的量分?jǐn)?shù))
(4)如果想進(jìn)一步提高H2S的轉(zhuǎn)化率,除改變溫度、壓強(qiáng)外,還可以采取的措施有___________________。
【答案】A + 2B ![]() 2C 升高溫度 a K1 > K2 = K3 > p3>p2>p1 1 及時分離出產(chǎn)物
2C 升高溫度 a K1 > K2 = K3 > p3>p2>p1 1 及時分離出產(chǎn)物
【解析】
Ⅰ.(1)根據(jù)3min達(dá)到平衡時A、B、C的物質(zhì)的量變化判斷反應(yīng)物、生成物,然后根據(jù)物質(zhì)的量變化與化學(xué)計(jì)量數(shù)成正比寫出反應(yīng)的化學(xué)方程式;
(2)①t3時正逆反應(yīng)速率同時增大,且逆反應(yīng)速率大于正反應(yīng)速率,說明平衡向著逆向移動,據(jù)此進(jìn)行判斷改變的反應(yīng)條件;
②根據(jù)a、b、c三點(diǎn)A的轉(zhuǎn)化率判斷產(chǎn)物C的體積分?jǐn)?shù)大小;
③化學(xué)平衡常數(shù)與溫度有關(guān),溫度越高,平衡向著逆向移動,該反應(yīng)的平衡常數(shù)減小;
Ⅱ.(1)恒壓條件下,溫度升高,H2S的轉(zhuǎn)化率升高;
(2) 依據(jù)化學(xué)平衡移動原理可知壓強(qiáng)增大平衡向氣體體積減小的方向進(jìn)行;
(3) 結(jié)合化學(xué)平衡三行計(jì)算列式計(jì)算平衡物質(zhì)的物質(zhì)的量,用平衡分壓代替平衡濃度計(jì)算,分壓=總壓×物質(zhì)的量分?jǐn)?shù);
(4) 如果想進(jìn)一步提高H2S的轉(zhuǎn)化率,除改變溫度、壓強(qiáng)外,可以減少生成物濃度促進(jìn)平衡正向進(jìn)行,提高硫化氫的轉(zhuǎn)化率。
Ⅰ.(1)根據(jù)圖象可知,達(dá)到平衡時A的物質(zhì)的量減小了:1mol-0.7mol=0.3mol,B的物質(zhì)的量減小為:1mol-0.4mol=0.6mol,C的物質(zhì)的量增加,增加的物質(zhì)的量為:0.6mol,所以A、B、C的物質(zhì)的量變化之比為:0.3mol:0.6mol:0.6mol=1:2:3,該反應(yīng)的化學(xué)方程式為:A+2B![]() 2C;
2C;
(2)①根據(jù)圖象可知:t3時正逆反應(yīng)速率同時增大,且逆反應(yīng)速率大于正反應(yīng)速率,說明平衡向著逆向移動,若增大壓強(qiáng),平衡向著正向移動,由于該反應(yīng)為放熱反應(yīng),升高溫度后平衡向著逆向移動,所以t3時升高了溫度;
②根據(jù)圖象變化可知,在t1~t2時反應(yīng)向著正向移動,A轉(zhuǎn)化率逐漸增大,直至t2~t3時反應(yīng)達(dá)到平衡狀態(tài),A轉(zhuǎn)化率達(dá)到最大;而t3~t4時升高了溫度,平衡向著逆向移動,A的轉(zhuǎn)化率逐漸減小,直至t4~t5時A的轉(zhuǎn)化率達(dá)到最低;而t5~t6時正逆反應(yīng)速率同時增大且相等,說明平衡沒有移動,A的轉(zhuǎn)化率不變,與t4~t5時相等,所以A的轉(zhuǎn)化率最大的時間段是:t2~t3,A的轉(zhuǎn)化率最大時C的體積分?jǐn)?shù)最大,此時間段為t2~t3,即為a點(diǎn);
③反應(yīng)A+2B2C △H<0,溫度升高平衡向著逆反應(yīng)方向移動,化學(xué)平衡常數(shù)減小,所以溫度越高,化學(xué)平衡常數(shù)越小;t2~t3、t3~t4、t4~t5時間段的溫度關(guān)系為:t3~t4=t4~t5>t2~t3,所以化學(xué)平衡常數(shù)大小關(guān)系為:K1>K2=K3。
Ⅱ. (1) 恒壓條件下,溫度升高,H2S的轉(zhuǎn)化率升高,即升高溫度平衡正向移動,則△H> 0;
(2) 2H2S(g)![]() 2H2(g)+S2(g) △H=+169.8kJmol-1,反應(yīng)是氣體體積增大的反應(yīng),溫度不變,壓強(qiáng)增大平衡逆向進(jìn)行,H2S的轉(zhuǎn)化率減小,則壓強(qiáng)關(guān)系為:P1<P2<P3;
2H2(g)+S2(g) △H=+169.8kJmol-1,反應(yīng)是氣體體積增大的反應(yīng),溫度不變,壓強(qiáng)增大平衡逆向進(jìn)行,H2S的轉(zhuǎn)化率減小,則壓強(qiáng)關(guān)系為:P1<P2<P3;
(3) M點(diǎn)的H2S轉(zhuǎn)化率為50%,總壓為5MPa,設(shè)H2S起始量為2mol,
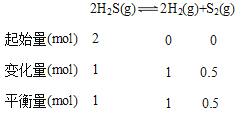
Kp=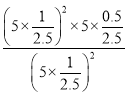 =1;
=1;
(4) 如果想進(jìn)一步提高H2S的轉(zhuǎn)化率,除改變溫度、壓強(qiáng)外,可以減少生成物濃度促進(jìn)平衡正向進(jìn)行,提高硫化氫的轉(zhuǎn)化率,采取的措施有及時分離出產(chǎn)物。


 唐印文化課時測評系列答案
唐印文化課時測評系列答案 導(dǎo)學(xué)與測試系列答案
導(dǎo)學(xué)與測試系列答案
| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:
【題目】氮可以形成多種離子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+與N2H62+是由中性分子結(jié)合質(zhì)子形成的,類似于NH4+,因此有類似于NH4+的性質(zhì)。
⑴寫出N2H62+在堿性溶液中反應(yīng)的離子方程式_________;
⑵NH2-的電子式為_________;
⑶N3-有_______個電子;
⑷寫出二種由多個原子組成的含有與N3-電子數(shù)相同的物質(zhì)的化學(xué)式_________;
⑸等電子數(shù)的微粒往往具有相似的結(jié)構(gòu),試預(yù)測N3-的構(gòu)型_________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】實(shí)驗(yàn)室利用如圖裝置進(jìn)行中和熱的測定。回答下列問題:
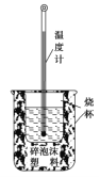
(1)該圖中有兩處未畫出,它們是 ____________、_______________;
(2)在操作正確的前提下提高中和熱測定的準(zhǔn)確性的關(guān)鍵是____________________;
(3)如果用50 mL0.50 mol/L的鹽酸和0.03 mol氫氧化鈉固體進(jìn)行實(shí)驗(yàn),則實(shí)驗(yàn)中所測出的“中和熱”的熱值將____________(填“偏大”、“偏小”或“不變”);
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】納米級Cu2O由于具有優(yōu)良的催化性能而受到關(guān)注,下表為制取Cu2O的兩種方法:
方法a | 用炭粉在高溫條件下還原CuO |
方法b | 電解法,反應(yīng)為2Cu+H2O |
(1)工業(yè)上常用方法b制取Cu2O而很少用方法a,其原因是反應(yīng)條件不易控制,若控溫不當(dāng)易生成__________而使Cu2O產(chǎn)率降低。
(2)已知:①2Cu(s)+ ![]() O2(g)=Cu2O(s) ΔH1=-169 kJ·mol-1
O2(g)=Cu2O(s) ΔH1=-169 kJ·mol-1
②C(s)+ ![]() O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
③Cu(s)+ ![]() O2(g)=CuO(s) ΔH3=-157 kJ·mol-1
O2(g)=CuO(s) ΔH3=-157 kJ·mol-1
則方法a中發(fā)生的反應(yīng):2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=________。
(3)方法b是用肼燃料電池為電源,通過離子交換膜電解法控制電解液中OH-的濃度來制備納米Cu2O,裝置如圖所示:
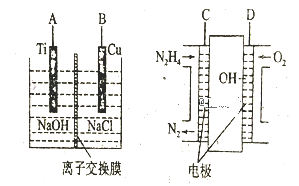
①上述裝置中B電極應(yīng)連_________電極(填“C”或“D”)。
②該離子交換膜為____離子交換膜(填“陰”或“陽”),該電解池的陽極反應(yīng)式為_______。
③原電池中負(fù)極反應(yīng)式為______________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】(1)亞硝酰氯(ClNO)是有機(jī)合成中常用試劑,已知:2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0,一定溫度下,將2 molNO與2 molCl2置于2L密閉容器中發(fā)生反應(yīng)。
2ClNO(g) △H<0,一定溫度下,將2 molNO與2 molCl2置于2L密閉容器中發(fā)生反應(yīng)。
①下列可判斷反應(yīng)達(dá)平衡狀態(tài)的是___________(填序號字母)。
A. 混合氣體的平均相對分子質(zhì)量不變 B. 混合氣體密度保持不變
C. NO和Cl2的物質(zhì)的量之比保持不變 D. 每消耗1 moI NO同時生成1molClNO
②為了加快化學(xué)反應(yīng)速率,同時提高NO的轉(zhuǎn)化率,其他條件不變時,可采取的措施有_________(填選項(xiàng)序號字母)。
A. 升高溫度 B. 縮小容器體積 C. 再充入Cl2氣體 D. 使用合適的催化劑
③一定條件下在恒溫恒容的密閉容器中,按一定比例充入NO(g)和Cl2(g),平衡時ClNO的體積分?jǐn)?shù)隨n(NO)/n(Cl2)的變化圖像如圖(B)所示,當(dāng)n(NO)/n(Cl2)=2.5時,達(dá)到平衡狀態(tài),ClNO的體積分?jǐn)?shù)可能是下圖中D、E、F三點(diǎn)中的________點(diǎn)。
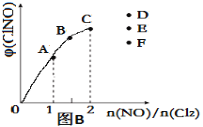
(2) 在體積為10 L的密閉容器中充入3 mol NO和2 mol Cl2,在不同溫度下發(fā)生反應(yīng)2NO(g)+Cl2(g)![]() 2ClNO(g),ClNO的百分含量隨時間的變化如圖所示。已知T1>T2>T3。
2ClNO(g),ClNO的百分含量隨時間的變化如圖所示。已知T1>T2>T3。
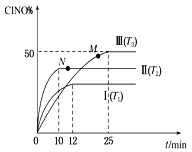
①與實(shí)驗(yàn)Ⅰ相比,實(shí)驗(yàn)Ⅱ除溫度不同外,還改變的條件是__________________。
②實(shí)驗(yàn)Ⅲ反應(yīng)至25 min達(dá)到平衡,用NO物質(zhì)的濃度變化表示的反應(yīng)速率為__________________。達(dá)到平衡時,若實(shí)驗(yàn)Ⅲ達(dá)到平衡時的熱量變化為Q kJ,則該反應(yīng)的熱化學(xué)方程式為________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】Ⅰ. 在容積為5L的密閉容器中,通入5 mol N2和8 mol H2,在一定條件下反應(yīng)生成NH3,當(dāng)反應(yīng)進(jìn)行到2 min時,測得容器內(nèi)有4 mol NH3。則:
(1)2 min時,容器內(nèi)n(N2)=________ ,c(H2)=___________。
(2)2 min時,容器內(nèi)氣體的總物質(zhì)的量與反應(yīng)前容器內(nèi)氣體的總物質(zhì)的量之比為 _______。
Ⅱ.在一定體積的密閉容器中進(jìn)行如下化學(xué)反應(yīng):CO2(g)+H2(g)![]() CO(g)+H2O(g),其化學(xué)平衡常數(shù)(K)和溫度(t)的關(guān)系如下表所示:
CO(g)+H2O(g),其化學(xué)平衡常數(shù)(K)和溫度(t)的關(guān)系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列問題:
(1)該反應(yīng)的化學(xué)平衡常數(shù)表達(dá)式為K=________。
(2)該反應(yīng)為________(填“吸熱”或“放熱”)反應(yīng)。
(3)能判斷該反應(yīng)達(dá)到化學(xué)平衡狀態(tài)的依據(jù)是________。
A.容器中壓強(qiáng)不變 B.混合氣體中c(CO)不變
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)某溫度下,平衡濃度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),試判斷此時的溫度為________ ℃。
(5)在800 ℃時,發(fā)生上述反應(yīng),某一時刻測得容器內(nèi)各物質(zhì)的濃度分別為c(CO2)為2 mol·L-1,c(H2)為1.5 mol·L-1,c(CO)為1 mol·L-1,c(H2O)為3 mol·L-1,則下一時刻,反應(yīng)將________(填“正向”或“逆向”)進(jìn)行
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】反應(yīng) 4A(s)+3B(g)![]() 2C(g)+D(g),經(jīng)2min 后,B的濃度減少了0.6molL-1。下列反應(yīng)速率的表示正確的是( )
2C(g)+D(g),經(jīng)2min 后,B的濃度減少了0.6molL-1。下列反應(yīng)速率的表示正確的是( )
A.用A表示的反應(yīng)速率是 0.4 mol·L-1·min-1
B.2min末時的反應(yīng)速率,用B表示為0.3 mol·L-1·min-1
C.用 B 表示的平均反應(yīng)速率是0.3 mol·L-1·min-1
D.在這 2 min 內(nèi),用 B 表示的反應(yīng)速率的值是減小的,用 C 表示的反應(yīng)速率逐漸增大
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下列有關(guān)元素及其化合物敘述中不正確的是( )
A.氧化鎂和氧化鋁熔點(diǎn)均很高,常用作耐高溫材料
B.在酒精燈加熱條件下,![]() 和
和![]() 固體都能分解
固體都能分解
C.二氧化氯具有氧化性,可用于自來水殺菌消毒
D.電閃雷鳴的雨天,![]() 與
與![]() 會發(fā)生反應(yīng)并最終轉(zhuǎn)化為硝酸鹽被植物吸收
會發(fā)生反應(yīng)并最終轉(zhuǎn)化為硝酸鹽被植物吸收
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
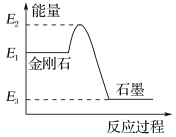
【題目】(1)我國成功發(fā)射的“天宮一號”飛行器的外殼覆蓋了一種新型結(jié)構(gòu)陶瓷材料,其主要成分是氮化硅,該陶瓷材料可由石英固體與焦炭顆粒在高溫的氮?dú)饬髦型ㄟ^如下反應(yīng)制得:3SiO2+6C+2N2![]() Si3N4+6CO,該反應(yīng)變化過程中的能量變化如圖所示。
Si3N4+6CO,該反應(yīng)變化過程中的能量變化如圖所示。

回答以下問題。
(1)該反應(yīng)________(填“吸熱”或“放熱”),反應(yīng)熱ΔH________0(填“>”、“<”或“=”)。
(2)已知:
As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+![]() O2(g)=As2O5(s) ΔH3
O2(g)=As2O5(s) ΔH3
則反應(yīng)As2O5(s)+3H2O(l)=2H3AsO4(s)的ΔH=__________。
(3)氮及其化合物在工農(nóng)業(yè)生產(chǎn)、生活中有著重要應(yīng)用,減少氮的氧化物在大氣中的排放是環(huán)境保護(hù)的重要內(nèi)容之一。已知:
①2NO(g)=N2(g)+O2(g) ΔH=-180.5 kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
③2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
某反應(yīng)的平衡常數(shù)表達(dá)式為K=![]() ,寫出此反應(yīng)的熱化學(xué)方程式:____________。
,寫出此反應(yīng)的熱化學(xué)方程式:____________。
(4)甲烷的燃燒熱為890.3 kJ/ mol ,請寫出表示CH4燃燒熱的熱化學(xué)方程式_____________。
(5)由圖可知,金剛石的穩(wěn)定性________石墨的穩(wěn)定性(填“>”、“<”或“=”)。
(6)中和熱的測定裝置如圖所示:
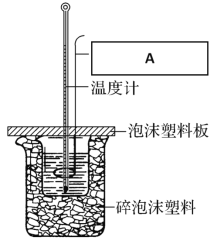
圖中A的儀器名稱:__________________作用:____________________________
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺 | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com