
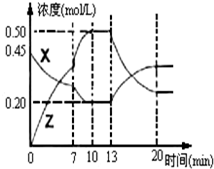
 I.在1L容器中通入CO2、H2各2mol,在一定條件下發生反應:CO2+H2?CO+H2O,回答下列問題:
I.在1L容器中通入CO2、H2各2mol,在一定條件下發生反應:CO2+H2?CO+H2O,回答下列問題:| 1×1 |
| 1×1 |
| 0.9×0.9 |
| 1.2×1.5 |


 輕松奪冠全能掌控卷系列答案
輕松奪冠全能掌控卷系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
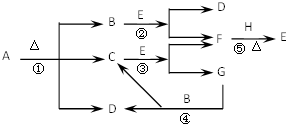 已知化合物A、D、E、G進行焰色反應時,火焰均呈黃色,其中A可用作家庭食品添加劑,也可用以治療胃酸過多.A~H各物質的變化關系如圖所示.
已知化合物A、D、E、G進行焰色反應時,火焰均呈黃色,其中A可用作家庭食品添加劑,也可用以治療胃酸過多.A~H各物質的變化關系如圖所示.| 氧化劑: | Na2O2 | 還原劑: | Na2O2 |
| 氧化產物: | O2 | 還原產物: | H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:
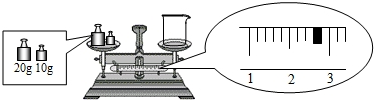
查看答案和解析>>
科目:高中化學 來源: 題型:
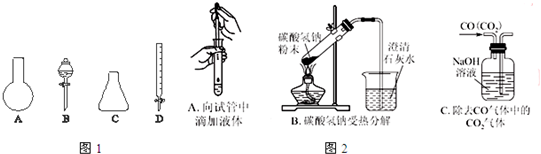
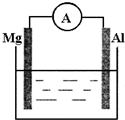 如圖所示裝置:
如圖所示裝置:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、將銅片加入到FeCl3溶液中,觀察溶液顏色的變化,證明微粒的氧化性Fe3+>Cu2+:Cu+2Fe3+=Cu2++2Fe2+ |
| B、測定0.1mol/LH3PO4溶液的pH>1證明H3PO4為弱酸:H3PO4?3H++PO43ˉ |
| C、實驗室用Na2O2與H2O反應,快速制備O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| D、向Na2CO3溶液中滴入甲基橙溶液,溶液變黃,證明Na2CO3溶液顯堿性:CO32ˉ+H2O?HCO3ˉ+OHˉ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com