
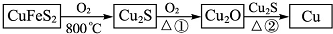
分析 (1)由題給信息知反應①是Cu2S和O2反應生成Cu2O的反應,由于Cu元素的化合價不變,O元素的化合價降低,則S元素的化合價一定升高,結合所學知識知道生成的物質為二氧化硫.化學方程式為同理,反應②是Cu2O和Cu2S反應生成Cu的反應,Cu元素的化合價降低,元素S的化合價升高生成二氧化硫,知道了反應物和生成物,配平化學方程式即可;
(2)Cu是29號元素,原子核外電子數為29,根據核外電子排布規律書寫銅的基態原子價電子排布式;同主族元素第一電離能自上而下逐漸減小;
(3)Si原子比C原子半徑大,Si、O原子間距離較大.
解答 解:(1)由題給信息知反應①是Cu2S和O2反應生成Cu2O的反應,由于Cu元素的化合價不變,O元素的化合價降低,則S元素的化合價一定升高,結合所學知識知道生成的物質為二氧化硫.化學方程式為2Cu2S+3O2=2Cu2O+2SO2;
反應②是Cu2O和Cu2S反應生成Cu的反應,Cu元素的化合價降低,元素S的化合價升高生成二氧化硫,化學方程式為2Cu2O+Cu2S═6Cu+SO2,
故答案為:2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S═6Cu+SO2;
(2)Cu是29號元素,原子核外電子數為29,銅的基態原子價電子電子排布式3d104s1,同主族元素第一電離能自上而下逐漸減小,所以第一電離能較大的是氧;
故答案為:3d104s1;氧;
(3)CO2中C與O原子間形成σ鍵和π鍵,SiO2中Si與O原子間不形成上述π鍵,是因Si原子比C原子半徑大,Si、O原子間距離較大,P-P軌道肩并肩重疊程度較小,不能形成上述穩定的π鍵,故答案為:Si原子比C原子半徑大,Si、O原子間距離較大,P-P軌道肩并肩重疊程度較小,不能形成上述穩定的π鍵.
點評 本題考查了化學方程式的書寫、核外電子排布的內容,綜合性較強,難度中等,氧化還原反應應根據化合價的升降總數相等進行配平解答.


 出彩同步大試卷系列答案
出彩同步大試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | XY | B. | X2Y3 | C. | XY2 | D. | X2Y |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 回收廢舊電池 | |
| B. | 將工廠煙囪加高,減少周圍大氣污染 | |
| C. | 開發利用氫能源 | |
| D. | 推廣使用無磷洗滌劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
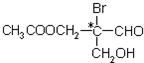 是某有機物分子的結構簡式,其中帶“*”的碳原子就是手性碳原子.當此有機物分別發生下列反應后,生成的有機物分子中仍含有手性碳原子的是( )
是某有機物分子的結構簡式,其中帶“*”的碳原子就是手性碳原子.當此有機物分別發生下列反應后,生成的有機物分子中仍含有手性碳原子的是( )| A. | 與乙酸發生酯化反應 | B. | 與NaOH水溶液反應 | ||
| C. | 催化劑作用下與H2反應 | D. | 與銀氨溶液作用發生銀鏡反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
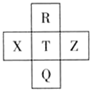 元素R、X、T、Z、Q在元素周期表中的相對位置如圖所示,其中R單質在暗處與H2劇烈化合并發生爆炸.則下列判斷正確的是( )
元素R、X、T、Z、Q在元素周期表中的相對位置如圖所示,其中R單質在暗處與H2劇烈化合并發生爆炸.則下列判斷正確的是( )| A. | 非金屬性:Z>T>X | B. | R與Q的電子數相差26 | ||
| C. | 氣態氫化物穩定性:R<T<Q | D. | R、T、Q的最高正價相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 將一塊鎂鋁的合金投入1mo1•L-1的一定體積的稀鹽酸中,待合金完全溶解后,往溶液里滴入1mo1•L-1的NaOH溶液,生成沉淀物質的量與加入NaOH溶液體積(單位mL)的關系如圖.下列說法中不正確的是( )
將一塊鎂鋁的合金投入1mo1•L-1的一定體積的稀鹽酸中,待合金完全溶解后,往溶液里滴入1mo1•L-1的NaOH溶液,生成沉淀物質的量與加入NaOH溶液體積(單位mL)的關系如圖.下列說法中不正確的是( )| A. | 由圖可以確定該鎂鋁合金中鋁的質量為0.27g | |
| B. | 當滴入1mo1•L-1的NaOH溶液85mL時,所得沉淀為Mg(OH)2和Al(OH)3 | |
| C. | 由圖可以確定a的取值范圍為:0≤a≤50 | |
| D. | 由圖可以確定該合金中鎂鋁物質的量之比0<$\frac{n(Mg)}{n(AI)}$<2.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應后的溶液的質量相同 | B. | 與濃硝酸的反應中,銅片先消失 | ||
| C. | 產生氣體的顏色相同 | D. | 產生氣體的體積相同(相同條件) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com