
| A. | 1.8g重水(D2O)中含有的質子數和電子數均為NA | |
| B. | 常溫下,16gO2和O3的混合氣體中含有的氧原子數為NA | |
| C. | 標準狀況下,22.4L NO和22.4LO2 混合后所得氣體中分子總數為1.5NA | |
| D. | 將11.2L Cl2通入足量的石灰乳中制備漂白粉,轉移的電子數為0.5NA |
分析 A、重水的摩爾質量為20g/mol;
B、氧氣和臭氧均由氧原子構成;
C、一氧化氮與氧氣反應生成二氧化氮,二氧化氮與四氧化二氮之間存在轉化平衡,所以反應后的物質中含有的分子數減小;
D、氯氣所處的狀態不明確.
解答 解:A、重水(D2O)的相對分子質量為20,1.8 g重水(D2O)的物質的量為0.09mol,含有的質子數和電子數均為0.9NA,故A錯誤;
B、氧氣和臭氧均由氧原子構成,16gO2和O3的混合氣體中氧原子的物質的量為1 mol,氧原子數為NA,故B正確;
C、根據2NO+O2═2NO2可知:標準狀況下,22.4 L NO即1molNO 和22.4 L O2 即1mol氧氣混合后所得氣體的物質的量為1.5mol,但由于NO2氣體中存在平衡:2NO2?N2O4,導致分子總數小于1.5 NA,故C錯誤;
D、缺少溫度和壓強,無法確定11.2 L Cl2的物質的量,無法確定轉移的電子數,故D錯誤.
故選B.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的運用以及物質的狀態和結構是解題關鍵,難度不大.


 巧學巧練系列答案
巧學巧練系列答案科目:高中化學 來源: 題型:選擇題
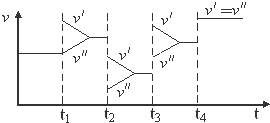
| A. | t1時改變的條件是增大體系的壓強 | B. | t2時改變的條件是減小壓強 | ||
| C. | t3時改變的條件是升高溫度 | D. | t4時改變的條件是使用了催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應①中還原產物只有SO2 | |
| B. | 反應②中Cu2S只發生了氧化反應 | |
| C. | 將1 molCu2S冶煉成 2mol Cu,需要O21mol | |
| D. | 若1molCu2S完全轉化為2molCu,則轉移電子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
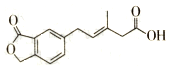
| A. | M可以發生加成、加聚、水解、酯化等反應 | |
| B. | l mol M最多可以與3 mol NaOH反應 | |
| C. | M苯環上的一氯取代物有兩種不同結構 | |
| D. | l molM最多可以與5 mol H2發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
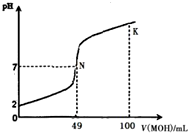 酸堿中和滴定是最基本的定量分析化學實驗.常溫下,向50mL 0.5mol•L-1 HA溶液中逐滴加入0.5mol•L-1強堿 MOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計).下列敘述正確的是( )
酸堿中和滴定是最基本的定量分析化學實驗.常溫下,向50mL 0.5mol•L-1 HA溶液中逐滴加入0.5mol•L-1強堿 MOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計).下列敘述正確的是( )| A. | 由圖中信息可知 HA為強酸,N點為恰好中和 | |
| B. | 常溫下一定濃度的 MA稀溶液的pH<7 | |
| C. | K點所對應的溶液中離子濃度的大小關系:c(M+)>c(OH-)>c(A-)>c(H+) | |
| D. | K點對應的溶液中,溶液的pH>13,c(HA)+c(A-)=0.25mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2COOH | B. | CH3COOCH3 | C. | HCOOCH2CH3 | D. | CH3COCH2OH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗序號 | 金屬 質量/g | 金屬狀態 | c(H2SO4) /mol•L-1 | V(H2SO4)/mL | 溶液溫度/℃ | 金屬消失的時間/s | |
| 反應前 | 反應后 | ||||||
| 1 | 0.10 | 絲 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 絲 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 絲 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 絲 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 絲 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 絲 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 絲 | 1.1 | 50 | 30 | 44 | 40 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 通過品紅溶液 | |
| B. | 通過澄清石灰水 | |
| C. | 先通過高錳酸鉀溶液,再通過澄清石灰水 | |
| D. | 先通過澄清石灰水,再通過高錳酸鉀溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com