
| 實際應用 | 相應性質 | |
| A | 用含有酸性重鉻酸鉀溶液的儀器檢驗酒后駕車 | 乙醇具有還原性 |
| B | 明礬常用于自來水的凈化、殺菌消毒 | 明礬可發生水解生成膠狀的Al(OH)3 |
| C | BaSO4可作為造影劑檢查腸胃道疾病 | BaSO4難溶于水且不與鹽酸反應 |
| D | 過氧化鈉可用作呼吸面具中的供氧劑 | Na2O2能與CO2反應生成O2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.酸性重鉻酸鉀具有氧化性,乙醇具有還原性;
B.明礬在溶液中電離出鋁離子水解生成氫氧化鋁膠體,能凈水;
C.BaSO4不溶于水和胃酸;
D.過氧化鈉與二氧化碳反應生成碳酸鈉和氧氣.
解答 解:A.酸性重鉻酸鉀具有氧化性,乙醇具有還原性,二者能發生氧化還原反應,該反應中乙醇作還原劑,表現還原性,故A正確;
B.明礬在溶液中電離出鋁離子水解生成氫氧化鋁膠體,氫氧化鋁膠體能吸附水中的懸浮顆粒,能凈水,但是不能殺菌消毒,故B錯誤;
C.BaSO4不溶于水和胃酸,所以BaSO4可作為造影劑檢查腸胃道疾病,故C正確;
D.過氧化鈉與二氧化碳反應生成碳酸鈉和氧氣,人呼出的氣體中含有二氧化碳,所以過氧化鈉可用作呼吸面具中的供氧劑,故D正確.
故選B.
點評 本題考查較綜合,涉及氧化還原反應、物質的性質和用途等知識點,明確基本原理、物質性質是解本題關鍵,側重于考查學生對基礎知識的應用能力,題目難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 化學反應中,化學能全部轉化為熱能 | |
| B. | 已知C(s)+$\frac{1}{2}$O2(g)═CO(g),△H=-110.5kJ•mol-1,則碳的燃燒熱為-110.5kJ•mol-1 | |
| C. | 測定中和熱時,用銅制攪拌棒代替環形玻璃攪拌棒不影響測定結果 | |
| D. | 反應C(s)+CO2(g)═2CO(g)△H>0在較高溫度下能自發進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 最高價含氧酸酸性:d>c>b | |
| B. | 它們均存在兩種或兩種以上的氧化物 | |
| C. | b與氫形成的化合物只存在極性共價鍵 | |
| D. | a、b、c的離子半徑依次增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在紫外線、飽和(NH4)2SO4溶液、CuSO4溶液等作用下,蛋白質均會發生變化 | |
| B. | 為檢驗皂化反應進行程度,取幾滴反應液,滴入裝有熱水的試管中,振蕩,若有油滴浮在液面上,說明油脂已完全反應 | |
| C. | 只用新制Cu(OH)2懸濁液就可以鑒別乙酸溶液、葡萄糖溶液、淀粉溶液 | |
| D. | 苯是從煤中分離得到的一種重要的化工原料,是無色、有特殊氣味的液態烴 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 陽離子 | K+、Cu2+、Fe3+、Ca2+、Fe2+ |
| 陰離子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
| A. | 溶液中一定含有的離子是K+、Cl-、CO32-、NO3-、SO42- | |
| B. | Ⅰ中加入鹽酸生成無色氣體的離子方程式是CO32-+2H+═CO2↑+H2O | |
| C. | 原溶液中的K+、Cl-、NO3-存在與否無法確定 | |
| D. | Ⅱ中產生白色沉淀的離子方程式是Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
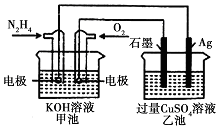
| A. | 該裝置工作時,Ag電極上有氣體生成 | |
| B. | 甲池和乙池中的溶液的pH均減小 | |
| C. | 甲池中負極反應為N2H4-4e-═N2+4H+ | |
| D. | 當甲池中消耗0.1molN2H4時,乙池中理淪上最多產生6.4g固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
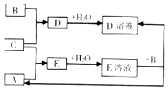 短周期元素X、Y、Z的原子序數依次增大,其中Y元素的原子半徑最大.已知A、B、C分別是X、Y、Z三種元素的單質,A和C常溫下為氣體.在適宜的條件下,A、B、C可以發生如圖所示的反應.下列說法正確的是( )
短周期元素X、Y、Z的原子序數依次增大,其中Y元素的原子半徑最大.已知A、B、C分別是X、Y、Z三種元素的單質,A和C常溫下為氣體.在適宜的條件下,A、B、C可以發生如圖所示的反應.下列說法正確的是( )| A. | 化合物YX中含離子鍵 | B. | Z的含氧酸均為強酸 | ||
| C. | 非金屬性:X>Z | D. | 離子半徑:Y>Z |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在濃硫酸作用下,60g冰醋酸與足量無水乙醇反應生成乙酸乙酯的分子數為NA | |
| B. | 標準狀況下,3.36LC2H4和C3H6的混合氣體中含有碳碳雙鍵的數目為0.15NA | |
| C. | 電解精煉銅,當外電路轉移NA個電子時,陽極質量減少32g | |
| D. | 含0.01molFeCl3的濃溶液滴入沸水,制得的膠體粒子數目小于0.01NA |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com