
分析 (1)根據n=$\frac{m}{M}$計算出二氧化錳的物質的量,再根據n=cV計算出100mL12mol/L濃鹽酸中含有HCl的物質的量,結合反應方程式判斷過量情況,根據不足量計算出生成氯氣的物質的量,最后根據V=nVm計算出生成氯氣在標準狀況下的體積;
(2)HCl被氧化生成氯氣,根據氯氣的物質的量及Cl鹽酸守恒計算出發生氧化反應的HCl的物質的量;
(3)加入過量硝酸銀溶液反應生成AgCl沉淀,根據Cl元素守恒可計算出生成氯化銀的物質的量,然后根據m=nM計算出生成氯化銀的質量.
解答 解:(1)10.44g二氧化錳的物質的量為:$\frac{10.44g}{87g/mol}$=0.12mol,100mL12mol/L濃鹽酸中含有HCl的物質的量為:12mol/L×0.1L=1.2mol,
根據反應MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O可知,0.12mol二氧化錳完全反應消耗HCl的物質的量為:0.12mol×4=0.48mol<1.2mol,說明濃鹽酸過量,生成的氯氣按照二氧化錳的量計算,
MnO2+4HCl(濃)→MnCl2+Cl2↑+2H2O
1 1
0.12mol n(Cl2)
則生成氯氣的物質的量為0.12mol,標準狀況下0.12mol氯氣的體積為:22.4L/mol×0.12mol=2.688L,
答:在標準狀況下生成2.688LCl2;
(2)反應MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中HCl被氧化生成氯氣,根據Cl元素守恒可知發生氧化反應的HCl的物質的量為:n(HCl)=2n(Cl2)=0.12mol×
2=0.24mol,
答:發生氧化反應的HCl的物質的量為0.24mol;
(3)100mL12mol/L濃鹽酸中含有HCl的物質的量為1.2mol,被氧化生成氯氣的HCl的物質的量為0.24mol,則反應后溶液中含有氯離子的物質的量為:1.2mol-0.24mol=0.96mol,
根據Cl元素守恒可知生成AgCl的物質的量為0.96mol,質量為:143.5g/mol×0.96mol=137.76g,
答:向反應后的溶液中加入過量的AgNO3溶液,則能生成137.76g AgCl白色沉淀.
點評 本題考查了氧化還原反應計算,題目難度中等,明確氧化還原反應的實質為解答關鍵,注意掌握守恒思想在化學計算中的應用,試題培養了學生的化學計算能力.


 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案科目:高中化學 來源: 題型:多選題
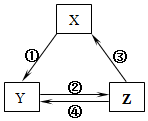 表所列各組物質中,物質之間通過一步反應就能實現如圖所示轉化且所給反應條件正確的是( )
表所列各組物質中,物質之間通過一步反應就能實現如圖所示轉化且所給反應條件正確的是( )| 選項 | X | Y | Z | 箭頭上所標數字的反應條件 |
| A | SiO2 | Na2SiO3 | H2SiO3 | ①與Na2CO3熔融 |
| B | Na | Na2O2 | NaCl | ②加H2O |
| C | NO | NO2 | HNO3 | ③與C加熱 |
| D | Al2O3 | NaAlO2 | Al(OH)3 | ④與NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cu(OH)2難溶于水,屬于非電解質 | |
| B. | Al2O3既能與強堿反應生成鹽和水又能與酸反應生成鹽和水,屬于兩性氧化物 | |
| C. | NH4Cl組成中不含金屬離子,不屬于鹽 | |
| D. | HCl氣體溶于水電離出H+和Cl-,屬于離子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D | |
| 氣體 | HCl | HCl | CO2 | SO2 |
| 液體 | H2O | NaOH | H2O | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | O2、O3是同一種單質 | |
| B. | 1H、2H、3H、H+、H2是氫元素形成的五種不同粒子 | |
| C. | 正丁烷和異丁烷互為同系物 | |
| D. | 乙醇、乙醚互為同分異構體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe2O3失電子 | B. | Al被還原 | ||
| C. | Fe2O3發生氧化反應 | D. | 每消耗27g鋁轉移3mol電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①⑥ | B. | ③⑥⑦⑩ | C. | ①②③⑩ | D. | ①④⑥⑦ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 青銅是我國用量最大、用途最廣的合金 | |
| B. | FeCl3腐蝕Cu刻制印刷電路板 | |
| C. | 硅膠可用作食品干燥劑 | |
| D. | SO2可用于漂白紙漿 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com