
分析 ①KMnO4溶液具有強氧化性,可以腐蝕橡皮管,故KMnO4溶液應裝在酸式滴定管中;
KMnO4溶液呈紫色,草酸反應完畢,滴入最后一滴KMnO4溶液,紫色不褪去,說明滴定到終點,不需要外加指示劑;
②由題給化學方程式及數據可得出X,若滴定用的KMnO4溶液因放置時間過長而部分變質,濃度偏低,則所得消耗酸性KMnO4溶液的體積偏大,由此所得n(H2C2O4)偏大,則n(H2O)偏小,x偏低;
③根據化學方程式及各物質之間的關系進行計算.
解答 解:①KMnO4溶液具有強氧化性,可以腐蝕橡皮管,故KMnO4溶液應裝在酸式滴定管中;
KMnO4溶液呈紫色,草酸反應完畢,滴入最后一滴KMnO4溶液,紫色不褪去,說明滴定到終點,不需要外加指示劑,
故答案為:酸;否;紫紅色KMnO4溶液被H2C2O4還原為Mn2+時溶液褪色、當最后一滴KMnO4滴入時,溶液中紫紅色不再褪去即為滴定終定;
②若滴定用的KMnO4溶液因放置時間過長而部分變質,濃度偏低,由此所得n(H2C2O4)偏大,則n(H2O)偏小,x偏低,
故答案為:偏低;
③由2MnO2-+5H2C2O4 +6H+═2Mn2++10CO2↑+8H2O
2mol 5mol
aV×10-3mol 0.025×Cmol
$\frac{2mol}{aV×1{0}^{-3}mol}$=$\frac{5mol}{0.025L×cmol/L}$
解得:C=$\frac{aV}{10}$mol•L-1
H2C2O4•xH2O~H2C2O4 ~xH2O
1mol 18xg
0.1aV×0.1 w-0.1aV×0.1×90
$\frac{1mol}{0.1aV×0.1}$=$\frac{18xg}{w-0.1aV×0.1×90}$
解得x=$\frac{50m-45aV}{9aV}$.
故答案為:$\frac{aV}{10}$;$\frac{50m-45aV}{9aV}$.
點評 本題考查了滴定操作、滴定應用與計算、物質組成含量測定等,難度題目中等,注意滴定中經常根據關系式進行計算,掌握根據關系式計算方法.


科目:高中化學 來源: 題型:推斷題
| 元素 | 相關信息 |
| X | X的最高價氧化為對應的水化物化學式為H2XO3 |
| Y | Y是地殼中含量最高的元素 |
| Z | Z的基態原子最外層電子排布式為3s23p1 |
| W | W的一種核素的質量數為28,中子數為14 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
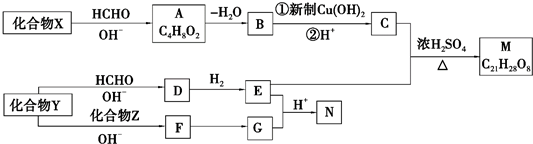
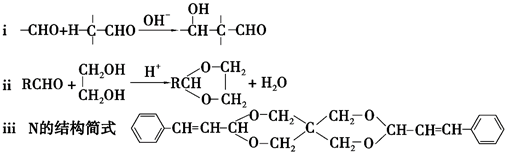
 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$ +Cu2O↓+3H2O.
+Cu2O↓+3H2O. .
.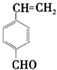 和
和 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 充電時,電解質溶液中K+向陽極移動 | |
| B. | 放電時,電解質溶液中K+向正極移動 | |
| C. | 充電時,陽極反應為:Zn(OH)${\;}_{4}^{2-}$+2e-═Zn+4OH- | |
| D. | 放電時,電路中通過2mol電子,消耗氧氣22.4L(標準狀況) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AlCl3溶液中加入過量氨水:Al3++4OH-=AlO2-+2H2O | |
| B. | 漂白粉溶液中通入適量的SO2氣體:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| C. | 用稀硝酸除去試管內壁銀:3Ag+4H++NO3-=3Ag++NO↑+2H2O | |
| D. | 澄清石灰水與少量小蘇打溶液混合:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 Ⅰ:A、B、W、D、E為短周期元素,且原子序數依次增大,質子數之和為39,B、W同周期,A、D同主族,A、W能形成兩種液態化合物A2W和A2W2,E元素的周期序數與主族序數相等.
Ⅰ:A、B、W、D、E為短周期元素,且原子序數依次增大,質子數之和為39,B、W同周期,A、D同主族,A、W能形成兩種液態化合物A2W和A2W2,E元素的周期序數與主族序數相等.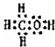 .
.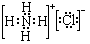 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | 熔點/℃ | 沸點/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題

| 溫度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| 溶解度/g | 41.6 | 47.5 | 53.8 | 61.3 | 70.5 | 75.4 | 71.1 | 60.5 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com