
| A. | 反應中有水參加反應 | |
| B. | 反應后溶液呈無色 | |
| C. | 該反應的還原劑為K2S2O8 | |
| D. | MnSO4和K2S2O8的化學計量數分別為、2 |
分析 根據反應物為硫酸錳(MnSO4)和過硫酸鉀(K2S2O8)兩種鹽溶液,生成物為高錳酸鉀、硫酸鉀和硫酸,利用質量守恒定律和電子守恒來寫出并配平上述反應的化學方程式為2MnSO4+5K2S2O8+8H2O=2KMnO4+4K2SO4+8H2SO4,Mn元素的化合價由+2價升高到+7價,則MnSO4為還原劑,S元素的化合價由+7降低為+6價,則K2S2O8為氧化劑,據此分析.
解答 解:A、由信息可知,反應物與生成物,則MnSO4+K2S2O8+H2O→KMnO4+K2SO4+8H2SO4,Mn元素的化合價由+2價升高到+7價,S元素的化合價由+7降低為+6價,
由電子守恒及質量守恒定律可知,配平的化學反應為2MnSO4+5K2S2O8+8H2O=2KMnO4+4K2SO4+8H2SO4,所以有水參加反應,故A正確;
B、因生成KMnO4為紫色,所以反應后溶液呈紫紅色,故B錯誤;
C、2MnSO4+5K2S2O8+8H2O=2KMnO4+4K2SO4+8H2SO4,Mn元素的化合價由+2價升高到+7價,則MnSO4為還原劑,S元素的化合價由+7降低為+6價,則K2S2O8為氧化劑,故C錯誤;
D、由2MnSO4+5K2S2O8+8H2O=2KMnO4+4K2SO4+8H2SO4,MnSO4和K2S2O8的化學計量數分別為2、5,故D錯誤;
故選:A.
點評 本題考查氧化還原反應,明確反應物與生成物并利用化合價的變化來寫反應方程式是解答本題的關鍵,并注意電子守恒的應用來解答此類習題.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 向氯化鋁溶液中加入過量稀氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | 向小蘇打溶液中加入醋酸溶液:HCO3-+CH3COOH═CH3COO-+CO2↑+H2O | |
| C. | 苯酚鈉溶液中通入二氧化碳CO2+H2O+2C6H5O-→2C6H5OH+CO32- | |
| D. | 向溴化亞鐵溶液中通入過量氯氣Fe2++2Br-+2Cl2═Fe3++Br2+4Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
 ,產物的結構簡式為
,產物的結構簡式為 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | △H1>△H2 | B. | △H2=△H1+△H4 | C. | △H3=△H2-△H5 | D. | △H4<0 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
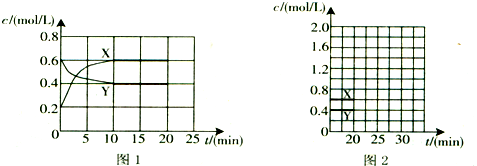
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1m ol | B. | 0.5mol | C. | 0.275mol | D. | 0.25mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
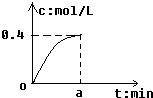 反應2SO2+O2?2SO3經amin后,SO3濃度的變化情況如圖所示,在時間0-amin內用O2表示的平均反應速率為0.04mol/(L•min),則a等于( )
反應2SO2+O2?2SO3經amin后,SO3濃度的變化情況如圖所示,在時間0-amin內用O2表示的平均反應速率為0.04mol/(L•min),則a等于( )| A. | 0.1 | B. | 2.5 | C. | 5 | D. | 10 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 130ml | B. | 100ml | C. | 90ml | D. | 50ml |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com