
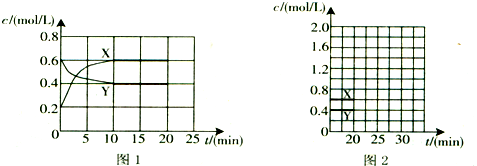
分析 由圖1可知,X、Y的濃度變化量之比為2:1,則X為NO2、Y為N2O4,發生反應:N2O4(g)?2NO2(g).
(1)A.隨反應進行混合氣體總物質的量增大,恒溫恒容下,容器內壓強增大,壓強不變說明到達平衡;
B.混合氣體總質量不變,容器的容積不變,密度始終不變;
C.容器內混合氣體的顏色不隨時間變化而改變,說明二氧化氮的濃度不變;
D.混合氣體總質量不變,隨反應進行混合氣體總物質的量增大,平均相對分子質量減小,平均相對分子質量不變說明到達平衡;
(2)反應進行到10min時,參加反應的四氧化二氮為1L×(0.6-0.4)mol/L=0.2mol,共吸收熱量11.38kJ,故反應1molN2O4共吸收熱量11.38kJ×5=56.9kJ,注明物質的聚集狀態與反應熱書寫熱化學方程式;
(3)平衡時c(NO2)=0.6mol/L、c(N2O4)=0.4mol/L,代入K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$計算;
(4)①恒溫恒容下,再充入一定量NO2,等效為增大壓強,平衡逆向移動;
②20min時瞬間c(NO2)增大,c(N2O4)不變,而后平衡向逆反應方向移動,c(NO2)減小,c(N2O4)增大,10min后達到新的平衡,此時測得c(NO2)=0.9mol/L,根據平衡常數計算平衡時c(N2O4),據此作圖.
解答 解:由圖1可知,X、Y的濃度變化量之比為2:1,則X為NO2、Y為N2O4,發生反應:N2O4(g)?2NO2(g).
(1)A.隨反應進行混合氣體總物質的量增大,恒溫恒容下,容器內壓強增大,壓強不變說明到達平衡,故A正確;
B.混合氣體總質量不變,容器的容積不變,密度為常數,密度不變不能說明到達平衡,故B錯誤;
C.NO2為紅棕色氣體,N2O4為無色氣體,容器內混合氣體的顏色不隨時間變化而改變,說明二氧化氮的濃度不變,反應到達平衡,故C正確;
D.混合氣體總質量不變,隨反應進行混合氣體總物質的量增大,平均相對分子質量減小,平均相對分子質量不變說明到達平衡,故D正確,
故選:B;
(2)反應進行到10min時,參加反應的四氧化二氮為1L×(0.6-0.4)mol/L=0.2mol,共吸收熱量11.38kJ,故反應1molN2O4共吸收熱量11.38kJ×5=56.9kJ,故該反應熱化學方程式為:N2O4(g)?2NO2(g),△H=+56.9kJ/mol,
故答案為:N2O4(g)?2NO2(g)△H=+56.9kJ/mol;
(3)平衡時c(NO2)=0.6mol/L、c(N2O4)=0.4mol/L,則平衡常數K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$=$\frac{0.{6}^{2}}{0.4}$=0.9,
故答案為:0.9;
(4)①恒溫恒容下,再充入一定量NO2,等效為增大壓強,平衡逆向移動,新平衡后混合氣體中NO2的體積分數減小,故W1>W2,故答案為:>;
②20min時瞬間c(NO2)增大,c(N2O4)不變,而后平衡向逆反應方向移動,c(NO2)減小,c(N2O4)增大,10min后達到新的平衡,此時測得c(NO2)=0.9mol/L,由于K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$=0.9,則平衡時c(N2O4)=$\frac{0.{9}^{2}}{0.9}$mol/L=0.9mol/L,而X為NO2、Y為N2O4,20min后各物質的濃度隨時間變化的曲線為: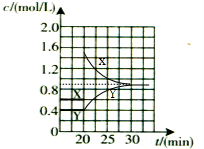 ,故答案為:
,故答案為: .
.
點評 本題考查化學平衡計算與影響因素、化學平衡狀態判斷、平衡常數等,(4)中作圖為易錯點,注意再次平衡時各物質的濃度、條件改變瞬間各物質的濃度,難度中等.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | -483.6kJ•mol-1 | B. | -241.8kJ•mol-1 | C. | -120.6kJ•mol-1 | D. | +241.8kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
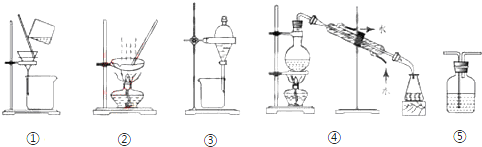
| A. | 分離Na2CO3溶液和CH3COOC2H5,選③ | B. | 用CCl4提取碘水中的碘,選② | ||
| C. | 實驗室中蒸餾水的制取,選④ | D. | 粗鹽提純,選②和③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 測定溶液pH時,pH試紙先用蒸餾水潤濕 | |
| B. | 蒸餾實驗中,蒸餾前必須在蒸餾燒瓶中加入碎瓷片 | |
| C. | 用鹽酸滴定滴定氨水實驗中,用甲基橙作指示劑以減小實驗誤差 | |
| D. |  用如圖所示的方法排除堿式滴定管膠管中的氣泡 用如圖所示的方法排除堿式滴定管膠管中的氣泡 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題

| A. | 能與FeCl3溶液發生顯色反應 | |
| B. | 該分子中含有3個手性碳原子 | |
| C. | 該化合物可與Br2發生取代反應 | |
| D. | 1mol該化合物最多可與5molNaOH反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應中有水參加反應 | |
| B. | 反應后溶液呈無色 | |
| C. | 該反應的還原劑為K2S2O8 | |
| D. | MnSO4和K2S2O8的化學計量數分別為、2 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | Fe2O3、Fe3O4、FeO | B. | FeO、Fe3O4 | C. | Fe3O4、Fe2O3 | D. | FeO、Fe2O3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com