
科學家開發出一種新型鋰-氧電池,其能量密度極高,效率達到90%以上,電池中添加碘化鋰(LiI)和微量水,工作原理如圖所示,總反應為:O2+4LiI+2H2O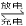 2I2+4LiOH對于該電池的下列說法不正確的是( )
2I2+4LiOH對于該電池的下列說法不正確的是( )
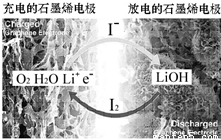
A.充電時陰極反應為LiOH+e-═Li+OH-
B.充電時Li+從陽極區移向陰極區
C.放電時正極反應為O2+2H2O+4Li++4e-═4LiOH
D.放電時負極上I-被氧化
科目:高中化學 來源:2016屆江蘇省等三校高三第四次模擬化學試卷(解析版) 題型:選擇題
根據下列實驗操作和現象所得出的結論正確的是
選項 | 實驗操作 | 實驗現象 | 結論 |
A | 向硅酸鈉溶液中滴加鹽酸 | 有白色膠狀沉淀生成 | 非金屬性:C1>Si |
B | 向溶液X中加入稀鹽酸,并將產生的無色無味氣體通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有CO32-或HCO3- |
C | 蔗糖溶液在硫酸存在下加熱一段時間后,再與銀氨溶液混合水浴加熱 | 無銀鏡出現 | 蔗糖沒有水解 |
D | 向雞蛋白溶液中滴入HgCl2溶液 | 有白色沉淀 | 蛋白質發生鹽析 |
查看答案和解析>>
科目:高中化學 來源:2016屆河北省高三下學期猜題理綜化學試卷(解析版) 題型:填空題
鋰離子電池廣泛應用于日常電子產品中,也是電動汽車動力電池的首選.正極材料的選擇決定了鋰離子電池的性能.磷酸鐵鉀(LiFePO4)以其高倍率性、高比能量、高循環特性、高安全性、低成本、環保等優點而逐漸成為“能源新星”。
(1)高溫固相法是磷酸鐵鋰生產的主要方法。通常以鐵鹽、磷酸鹽和鋰鹽為原料,按化學計量比充分混勻后,在惰性氣氛的保護中先經過較低溫預分解,再經高溫焙燒,研磨粉碎制成。其反應原理如下:
Li2CO3+2FeC2O4•2H2O+2NH4H2PO4═2NH3↑+3CO2↑+______+_______+_______
①完成上述化學方程式.
②理論上,反應中每轉移0.15mol電子,會生成LiFePO4______________g;
③反應需在惰性氣氛的保護中進行,其原因是______________;
(2)磷酸亞鐵鋰電池裝置如圖所示,其中正極材料橄欖石型LiFePO4通過粘合劑附著在鋁箔表面,負極石墨材料附著在銅箔表面,電解質為溶解在有機溶劑中的鋰鹽。
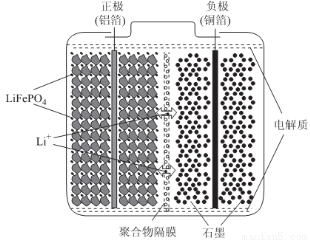
電池工作時的總反應為:LiFePO4+6C Li1-xFePO4+LixC6,則放電時,正極的電極反應式為______________。充電時,Li+遷移方向為______________(填“由左向右”或“由右向左”),圖中聚合物隔膜應為______________(填“陽”或“陰”)離子交換膜。
Li1-xFePO4+LixC6,則放電時,正極的電極反應式為______________。充電時,Li+遷移方向為______________(填“由左向右”或“由右向左”),圖中聚合物隔膜應為______________(填“陽”或“陰”)離子交換膜。
(3)用該電池電解精煉銅。若用放電的電流強度I=2.0A的電池工作10分鐘,電解精煉銅得到銅0.32g,則電流利用效率為______________(保留小數點后一位)。(已知:法拉第常數F=96500C/mol,電流利用效率= 100%)
100%)
(4)廢舊磷酸亞鐵鋰電池的正極材料中的LiFePO4難溶于水,可用H2SO4和H2O2的混合溶液浸取,發生反應的離子方程式為______________。
查看答案和解析>>
科目:高中化學 來源:2016屆山東省高三高考打靶測試理綜化學試卷(解析版) 題型:選擇題
全釩氧化還原電池是一種新型可充電池,不同價態的含釩離子作為正極和負極的活性物質,分別儲存在各自的酸性電解液儲罐中。其結構原理如圖所示,該電池放電時,右槽中的電極反應為:V2+-e-=V3+,下列說法正確的是( )
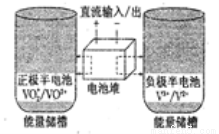
A.放電時,右槽發生還原反應
B.放電時,左槽的電極反應式:VO2++2H++e-=VO2++H2O
C.充電時,每轉移1mol電子,n(H+)的變化量為1mol
D.充電時,陰極電解液pH升高
查看答案和解析>>
科目:高中化學 來源:2016屆遼寧省高三全真模擬理綜化學試卷(解析版) 題型:填空題
【化學選修2:化學與技術】硝酸銨可用作化肥、軍用炸藥、殺蟲劑、冷凍劑等。工業制取硝酸銨的工藝流程如下:

(1)合成氨氣的工業設備名稱_______________,設備中設置熱交換器的目的是____________,合成氨的原料氣必須先脫硫,目的是_______________;
(2)吸收塔中反應的化學方程式為_________________________,從生產流程看,吸收塔中需要補充空氣,其原因是_______________;
(3)生產硝酸的過程中常會產生氮的氧化物,可用如下三種方法處理:
方法一:堿性溶液吸收法
NO+NO2+2NaOH═2NaNO2+H2O;2NO2+Na2CO3═NaNO2+NaNO3+CO2
方法二:NH3還原法
8NH3(g)+6NO2(g)═7N2(g)+12H2O(g)△H=-2635kJ/mol(NO也有類似的反應)
方法三:甲烷吸收法
CH4(g)+2NO2═CO2(g)+N2+2H2O(g)△H=+867kJ/mol(NO也有類似的反應)
上述三種方法中,方法一的主要缺點是_______________;
方法三和方法二相比,方法三的缺點是_______________;
(4)工業上也可以通過電解NO制備NH4NO3,其工作原理如圖所示.

①圖中通入NH3的目的是_______________;
②若維持電流強度為3A,電解2小時,理論上可制得NH4NO3的最大質量為_____g;(已知F=96500C•mol-l)(保留2位有效數字).
(5)某化肥廠用NH3制備NH4NO3.己知:NH3制NO的產率是94%,NO制HNO3的產率是89%,則制HNO3所用NH3的質量占總耗NH3質量(不考慮其他損耗)的百分比為______________。
查看答案和解析>>
科目:高中化學 來源:2016屆遼寧省高三全真模擬理綜化學試卷(解析版) 題型:選擇題
化學與材料、生活和環境密切相關。下列有關說法中錯誤的是( )
A.某新型航天服材料主要成分是由碳化硅、陶瓷和碳纖維復合而成,它是一種新型無機非金屬材料
B.瑪瑙飾品的主要成分與建筑材料砂子相同
C.明礬凈水時發生了化學及物理變化,能起到凈水作用,而沒有殺菌、消毒的作用
D.醫用酒精是利用了乙醇的氧化性來殺菌消毒的
查看答案和解析>>
科目:高中化學 來源:2016屆江西省高三考前熱身理綜化學試卷(解析版) 題型:選擇題
常溫下,向10ml 0.1 mol·L-1的HR溶液中逐滴滴入0.1mol·L-1的NH3·H2O溶液,所得溶液pH及導電性變化如圖。下列分析不正確的是
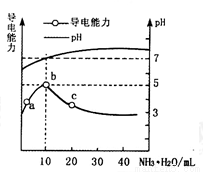
A.a~b點導電能力增強,說明HR為弱酸
B.c點溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+)
C.b點溶液pH=5,此時酸堿恰好中和
D.b~c任意點溶液均有c(H+)·c(OH-)=Kw=1.0×10-14
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三考前模擬理綜化學試卷(解析版) 題型:選擇題
已知在酸性溶液中,下列物質氧化 KI 時,自身發生如下變化:
ClO3一→ Cl一;MnO4一→ Mn2+;Cl2→2Cl一;IO3一 →I2。
如果分別用這些物質氧化的 KI生成等量的 I2,消耗他們物質的量最少的是( )
A.ClO3一 B.MnO4- C.Cl2 D.IO 3一
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省高二6月月考化學試卷(解析版) 題型:選擇題
下列關于Na2CO3和NaHCO3的性質的比較中,不正確的是
A.熱穩定性:Na2CO3>NaHCO3
B.常溫時的溶解度:NaHCO3<Na2CO3
C.與相同濃度稀鹽酸反應的劇烈程度:Na2CO3>NaHCO3
D.等質量的固體與足量鹽酸反應放出CO2的質量NaHCO3>Na2CO3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com