
| A. | HCl | B. | CaCO3 | C. | H2O | D. | NaOH |
分析 HClO的電離常數小于H2CO3的第一級電離常數(Ka1)大于H2CO3的第二級電離常數(Ka2),說明酸性H2CO3>HClO>HCO3-,氯水中含有HCl和HClO,為了提高氯水中HClO的濃度,加入的物質應該和鹽酸反應而和次氯酸不反應,根據強酸制取弱酸分析解答.
解答 解:HClO的電離常數小于H2CO3的第一級電離常數(Ka1)大于H2CO3的第二級電離常數(Ka2),說明酸性 H2CO3>HClO>HCO3-,氯水中含有HCl和HClO,為了提高氯水中HClO的濃度,加入的物質應該和鹽酸反應而和次氯酸不反應,
A、加和鹽酸,抑制氯氣與水的反應,減小了次氯酸的濃度,故A錯誤;
B、根據酸性強弱知,加入CaCO3,鹽酸與碳酸鈣反應,促使氯氣與水的反應正向進行,而次氯酸不與碳酸鈣反應,次氯酸的濃度增大,故B正確;
C、加水溶液被稀釋,次氯酸的濃度減小,故C錯誤;
D、氫氧化鈉與鹽酸和次氯酸都反應,所以次氯酸的濃度減小,故D錯誤;故選B.
點評 本題考查了弱電解質的電離,明確酸的電離平衡常數與酸性強弱之間關系是解本題關鍵,題目難度不大.


 期末集結號系列答案
期末集結號系列答案科目:高中化學 來源: 題型:填空題
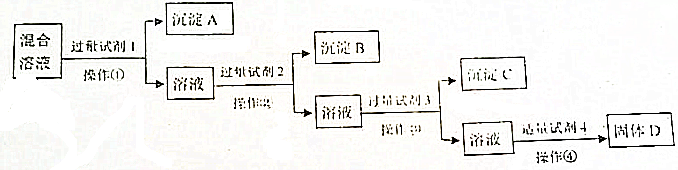
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用無磷洗衣粉,可徹底解決水體富營養化問題 | |
| B. | SO2是大氣污染物,可以用生石灰除去工業廢氣中的SO2 | |
| C. | 明礬水解產生Al(OH)3膠體粒子,可除去懸浮物 | |
| D. | 使用清潔能源是防止酸雨發生的重要措施之一 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,1mol CO2和CO混合氣體含有的碳原子數為NA | |
| B. | 在KIO3+6HI═KI+3I2+3H2O反應中,每生成 3molI2,則轉移6NA個電子 | |
| C. | 78gNa2O2與足量的CO2完全反應,轉移的電子總數為NA | |
| D. | 在1L0.1mol-L-1 Na2S溶液中,陰離子總數大于0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
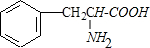 .
.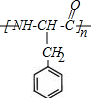 .
.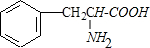 $→_{△}^{催化劑}$
$→_{△}^{催化劑}$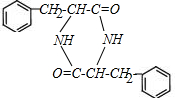 +2H2O;M與乙醇在濃硫酸、加熱條件下發生反應的類型為酯化反應(取代反應).
+2H2O;M與乙醇在濃硫酸、加熱條件下發生反應的類型為酯化反應(取代反應).查看答案和解析>>
科目:高中化學 來源: 題型:填空題

 (填分子式),其原因是在雙氧水分子中每個H原子和O原子形成一對共用電子對,O原子之間共用一對電子,這樣每個原子都達到穩定結構.
(填分子式),其原因是在雙氧水分子中每個H原子和O原子形成一對共用電子對,O原子之間共用一對電子,這樣每個原子都達到穩定結構.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
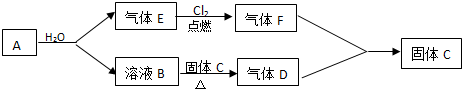
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com