
分析 (1)由離子交換關系,氫氧根離子物質的量等于氯離子物質的量等于氫離子物質的量,再計算Fe原子物質的量,根據Fe、Cl原子數目之比計算x的值;
(2)根據元素守恒計算氯化亞鐵和氯化鐵物質的量之比,進而計算氯化鐵質量分數;
(3)FeCl3具有氧化性,再溶液中將二氧化硫氧化為硫酸,自身還原為亞鐵離子;
(4)用FeCl3與KClO在強堿性條件下反應制取K2FeO4,氯元素被還原為氯離子,同時有水生成,配平書寫離子方程式;
K2FeO4-Zn也可以組成堿性電池,K2FeO4在電池中作為正極材料,負極為鋅失電子發生氧化反應.
解答 解:(1)n(Cl)=n(Cl-)=n(H+)=n(OH-)=0.06L×1 mol•L-1=0.06 mol,則m(Fe)=3.25g-0.06 mol×35.5g•mol-1=1.12g,故 n(Fe)=1.12g÷56g•mol-1=0.02 mol,所以 n(Fe):n(Cl)=0.02:0.06=1:3,即x=3,故答案為:3;
(2)設混合物中FeCl2物質的量為x,FeCl3的物質的量為y,則(x+y):(2x+3y)=1:2.8,得到x:y=1:4,氯化鐵物質的量分數=$\frac{4}{1+4}$×100%=80%,故答案為:80%;
(3)FeCl3具有氧化性,再溶液中將二氧化硫氧化為硫酸,自身還原為亞鐵離子,反應離子方程式為:SO2+2Fe3++H2O=SO42-+2Fe2++4H+,故答案為:SO2+2Fe3++H2O=SO42-+2Fe2++4H+;
(4)用FeCl3與KClO在強堿性條件下反應制取K2FeO4,氯元素被還原為氯離子,同時有水生成,反應的離子方程式為:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,
原電池的正極發生發生還原反應,負極發生氧化反應,負極電極反應為:Zn-2e-+2OH-=Zn(OH)2,正極電極反應式為:2FeO42-+6e-+8H2O=2Fe(OH)3+10OH-,
故答案為:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O;3Zn-6e-+6OH-=3Zn(OH)2;2FeO42-+6e-+8H2O=2Fe(OH)3+10OH-.
點評 本題考查滴定計算、混合物計算、離子方程式、原電池等,側重考查學生綜合知識應用能力,需要學生具備扎實的基礎,難點是電極反應式書寫,難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用燃燒的方法鑒別真絲圍巾和純棉圍巾 | |
| B. | 在烹調中加料酒和食醋,增加食物的香味 | |
| C. | 用工業酒精兌制飲用酒出售來提高利潤 | |
| D. | 食用加碘鹽,預防因缺碘引起的甲狀腺腫大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 17:5 | B. | 11:3 | C. | 3:1 | D. | 4:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
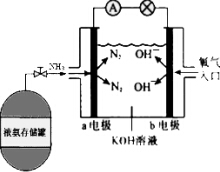 氨作為一種富氫化合物,具有各種優點,特別是氨有著良好的產業基礎,價格低廉,氨作為燃料電池燃料具有很大的發展潛力.氨氧燃料電池示意圖,回答下列問題.
氨作為一種富氫化合物,具有各種優點,特別是氨有著良好的產業基礎,價格低廉,氨作為燃料電池燃料具有很大的發展潛力.氨氧燃料電池示意圖,回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,pH=13的NaOH溶液與pH=1的醋酸溶液等體積混合后所得溶液的pH>7 | |
| B. | 疊氮酸(HN3)與醋酸酸性相似,NaN3水溶液中離子濃度大小順序為c(Na+)>c(N3-)>c(OH-)>c(H+) | |
| C. | 常溫下,向氨水中逐滴滴入鹽酸至溶液的pH=7,則混合液中c(NH4+)=c(Cl-) | |
| D. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
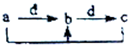 下表各組物質中,物質之間不能通過一步反應實現如圖所示轉化的( )
下表各組物質中,物質之間不能通過一步反應實現如圖所示轉化的( )| 物質 選項 | a | b | c | d |
| A | Al | Al(OH)3 | NaAlO2 | NaOH |
| B | C | CO | CO2 | O2 |
| C | NaOH | Na2CO3 | NaHCO3 | CO2 |
| D | AlCl3 | Al(OH)3 | NaAlO2 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 離子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 濃度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com