
分析 (1)反應物中的原子全部參加反應的,原子利用律最高,據此解答即可;水電離的OH-的物質的量濃度=$\frac{1{0}^{-14}}{1{0}^{-PH}}$;常溫下,0.1mol•L-1 KHCO3溶液pH>8,說明碳酸氫根在水解程度大于電離程度;
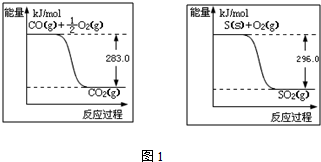
(2)由圖1可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
利用蓋斯定律(i)-(ii)計算即可;
(3)①根據時段Ⅰ達到平衡時生成氨氣的物質的量及熱化學方程式N2(g)+3H2(g)?2NH3(g);△H=-94.4kJ•mol-1計算出放出的熱量;
②根據25min時氨氣的物質的量變為0,而氮氣和氫氣的物質的量不變進行解答,改變的條件是分離出氨氣;
③根據時段Ⅲ條件下達到平衡時各組分的濃度及平衡常數等于生成物平衡濃度冪次方乘積除以反應物平衡濃度冪次方乘積進行解答;
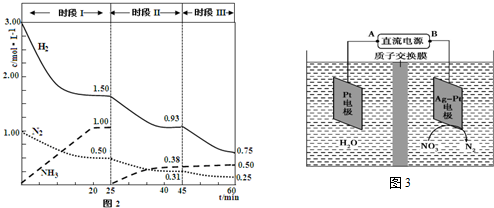
(4)由圖示知在Ag-Pt電極上NO3-發生還原反應,因此Ag-Pt電極為陰極,則B為負極,A為電源正極;在陰極反應是NO3-得電子發生還原反應生成N2,利用電荷守恒與原子守恒知有氫離子參與反應且有水生成.
解答 解:(1)觀察四個反應方程式可見,只有反應d中參加反應的物質全部轉化為一種物質,故原子利用率最高;
可用碳酸鉀溶液吸收生成的CO2,常溫下pH=10的碳酸鉀溶液中水電離的c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-PH}}$mol/L=1×10-4 mol•L-1;
常溫下,0.1mol•L-1 KHCO3溶液pH>8,則溶液中碳酸氫根離子水解程度大于電離程度,所以c(H2CO3)>c(CO32-);
故答案為:d; 1×10-4 mol•L-1;>;
(2)由圖1可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
(i)-(ii)得:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-563-(-298)=-270kJ•mol-1,
故答案為:-270kJ/mol;
(3)①時段Ⅰ達到平衡時生成的氨氣的物質的量為:1.00 mol/L×2L=2.00mol,
根據N2(g)+3H2(g)?2NH3(g);△H=-94.4kJ•mol-1可知生成2.00mol氨氣放出的熱量為94.4kJ,
故答案為:94.4kJ;
②25min時氨氣的物質的量迅速變為0而氮氣、氫氣的物質的量不變,之后氮氣、氫氣的物質的量逐漸減小,氨氣的物質的量逐漸增大,說明25min時改變的條件是將NH3從反應體系中分離出去,
故答案為:將NH3從反應體系中分離出去;
③時段Ⅲ條件下,反應為:N2(g)+3H2(g)?2NH3(g),圖象方向可知平衡狀態下[N2]=0.25mol/L,[NH3]=0.50mol/L,[H2]=0.75mol/L,該反應的化學平衡常數為:K=$\frac{{c}^{2}(N{H}_{3})}{{c({N}_{2})c}^{3}({H}_{2})}$=$\frac{(0.50mol/L)^{2}}{(0.75mol/L)^{3}×0.25mol/L}$=2.37,
故答案為:2.37;
(4)由圖示知在Ag-Pt電極上NO3-發生還原反應,因此Ag-Pt電極為陰極,則B為負極,A為電源正極;在陰極反應是NO3-得電子發生還原反應生成N2,利用電荷守恒與原子守恒知有H2O參與反應且有水生成,
所以陰極上發生的電極反應式為:2NO3-+12H++10e-=N2↑+6H2O,
故答案為:A,2NO3-+12H++10e-=N2↑+6H2O.
點評 本題主要考查的是綠色化學的概念、蓋斯定律的應用、影響化學平衡的因素及電解池工作原理,題目難度中等,明確化學平衡常數的概念及計算方法是解題關鍵.


科目:高中化學 來源: 題型:解答題
 無機化合物可根據其組成和性質進行分類
無機化合物可根據其組成和性質進行分類| 物質類別 | 酸 | 堿 | 鹽 | 氧化物 | 氫化物 |
| 化學式 | ①HCl②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2SO4 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該元素為Mn元素 | B. | 該元素最高化合價為+7 | ||
| C. | 該元素屬于d區元素 | D. | 該元素原子最外層共有7個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
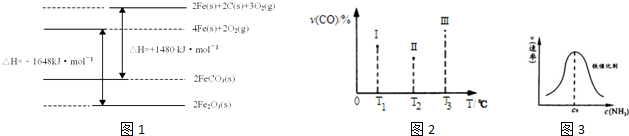
 分別表示N2、H2、NH3和固體催化劑,則在固體催化劑表面合成氨的過程可用圖表示:
分別表示N2、H2、NH3和固體催化劑,則在固體催化劑表面合成氨的過程可用圖表示:
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 2min | 4min | 6nin | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.20 | … |
| CH2OH | 0.03 | 0.04 | 0.04 | 0.05 | … |

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com