
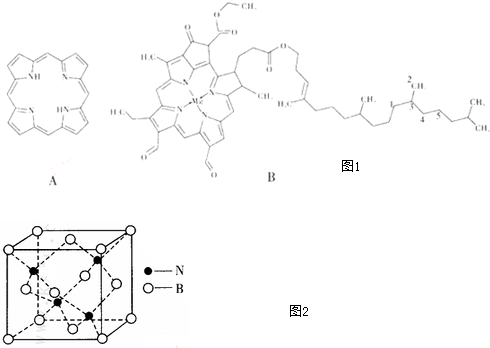
分析 (1)根據價層電子對互斥理論確定雜化方式;
(2)A.手性碳原子連接四個不同的原子或原子團;
B.含有孤電子對和含有空軌道的原子之間存在配位鍵;
C.結構甲烷、乙烯結構判斷是否共面;
D.同一周期元素,元素的第一電離能隨著原子序數增大而呈增大趨勢,但第IIA族、第VA族元素第一電離能大于其相鄰元素;
(3)Fe是26號元素,其原子核外有26個電子,失去兩個最外層電子生成亞鐵離子,根據構造原理書寫其核外電子排布式;
(4)HCN的結構式為H-C≡N,共價單鍵為σ鍵,共價三鍵中含有一個σ鍵兩個π鍵;極性分子的溶質極易溶于極性分子的溶劑;原子個數相等、價電子數相等的微粒互為等電子體;
(5)該晶胞中N原子個數為4、B原子個數=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,其化學式為BN,棱長為a×10-10cm,晶胞體積=(a×10-10cm)3,晶胞密度=$\frac{m}{V}$.
解答 解:(1)價層電子對個數是4的N原子采用sp3雜化、價層電子對個數是3的N采用sp2雜化,
故答案為:sp3、sp2;
(2)A.手性碳原子連接四個不同的原子或原子團,這幾個碳原子只有3號碳原子是手性碳原子,故錯誤;
B.含有孤電子對和含有空軌道的原子之間存在配位鍵,N原子含有孤電子對、中心原子含有空軌道,所以含有配位鍵,故正確;
C.結構甲烷、乙烯結構知,這幾個碳原子之間不能共面,故錯誤;
D.同一周期元素,元素的第一電離能隨著原子序數增大而呈增大趨勢,但第IIA族、第VA族元素第一電離能大于其相鄰元素,所以電負性N>O,故正確;
故選BD;
(3)Fe是26號元素,其原子核外有26個電子,失去兩個最外層電子生成亞鐵離子,根據構造原理書寫其核外電子排布式為1s22s22p63s23p63d6,故答案為:1s22s22p63s23p63d6;
(4)HCN的結構式為H-C≡N,共價單鍵為σ鍵,共價三鍵中含有一個σ鍵兩個π鍵,該分子中含有兩個σ鍵兩個π鍵,所以二者之比為1:1;
極性分子的溶質極易溶于極性分子的溶劑,HCN是極性分子、水是極性分子,所以HCN易溶于水;
原子個數相等、價電子數相等的微粒互為等電子體,CN-的等電子體有N2、CO等,
故答案為:1:1;易;HCN和水都是極性分子,根據相似相溶原理知,HCN易溶于水;N2、CO;
(5)該晶胞中N原子個數為4、B原子個數=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,其化學式為BN,棱長為a×10-10cm,晶胞體積=(a×10-10cm)3,晶胞密度=$\frac{m}{V}$=$\frac{\frac{M}{{N}_{A}}×4}{V}$=$\frac{\frac{25}{{N}_{A}}×4}{(a×1{0}^{-10})^{3}}$g.cm-3,
故答案為:$\frac{\frac{25}{{N}_{A}}×4}{(a×1{0}^{-10})^{3}}$.
點評 本題考查晶胞計算、相似相溶原理、電子排布、元素周期律及化學鍵等知識點,這些都是高頻考點,會利用價層電子對互斥理論、構造原理等知識點分析解答,難點是晶胞計算,知道密度公式中各個字母的含義,題目難度中等.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4+、Cl-、Na+、SO42- | B. | Na+、Ba2+、OH-、SO42- | ||
| C. | Ca2+、H+、S2-、ClO- | D. | H+、Cl-、Fe2+、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KMnO4溶液用鹽酸酸化并加入H2O2:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O | |
| B. | Fe2(SO4)3和Ba(OH)2溶液混合:Fe3++SO42-+Ba2++3OH-=BaSO4↓+Fe(OH)3↓ | |
| C. | 等體積等物質的量濃度的AlCl3、Ba(OH)2、HCl溶液混合:3H++Al3++6OH-=Al(OH)3↓+3H2O | |
| D. | 水玻璃與稀醋酸混合:SiO32-+2H+=H2SiO3↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
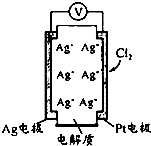 利用如圖所示原電池可測量空氣中Cl2含量,其中電解質是Ag+可以自由移動的固體物質.下列分析不正確的是( )
利用如圖所示原電池可測量空氣中Cl2含量,其中電解質是Ag+可以自由移動的固體物質.下列分析不正確的是( )| A. | 電子經外電路流向Pt電極 | |
| B. | 正極反應:Cl2+2e-+2Ag+=2AgCl | |
| C. | 電池工作時,電解質中Ag+數目減少 | |
| D. | 空氣中c(Cl2)越大,Ag極消耗速率越快 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 CO和H2作為重要的燃料和化工原料,有著十分廣泛的應用.
CO和H2作為重要的燃料和化工原料,有著十分廣泛的應用.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 224 mL | B. | 336 mL | C. | 448 mL | D. | 672 mL |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com