
分析 W、X、Y、Z是原子序數依次增大的同一周期元素,W、X是金屬元素,Y、Z是非金屬元素.
(1)W、X各自的氧化物對應的水化物可以反應生成鹽和水,可推知W為Na、X為Al;
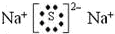
(2)W(Na)與Y可形成化合物W2Y,Y表現-2價,則Y為S;
(3)結合原子序數可知Z為Cl,S的低價氧化物通入氯氣的水溶液中,應為二氧化硫與氯氣反應生成硫酸與HCl;
(4)同周期自左而右元素非金屬性正確,非金屬性越強,氫化物越穩定;
(5)電子層結構相同核電荷數越大離子半徑越小,電子層越多離子半徑越大,據此判斷;
(6)Z的最高價氧化物為是Cl2O7,Cl2O7和水反應生成高氯酸,0.25molCl2O7和水反應放出QkJ熱量,則1molCl2O7和水反應放出4QkJ熱量.
解答 解:W、X、Y、Z是原子序數依次增大的同一周期元素,原子序數均小于18,W、X是金屬元素,Y、Z是非金屬元素
(1)W、X為金屬,其最高價氧化物對應的水化物為堿,且兩種堿可以反應生成鹽和水,則為NaOH和Al(OH)3,二者反應的離子方程式:Al(OH)3+OH-=AlO2-+2H2O,故答案為:Al(OH)3+OH-=AlO2-+2H2O;
(2)W(Na)與Y可形成化合物W2Y,Y表現-2價,則Y為S,Na2S的電子式為 ,故答案為:
,故答案為: ;
;
(3)結合原子序數可知Z為Cl,S的低價氧化物通入氯氣的水溶液中,應為二氧化硫與氯氣反應生成硫酸與HCl,反應化學方程式為SO2+Cl2+2H2O=H2SO4+2HCl,
故答案為:SO2+Cl2+2H2O=H2SO4+2HCl;
(4)同一周期元素中,元素的非金屬性隨著原子序數的增大而增強,元素的非金屬性越強,其氫化物越穩定,所以穩定性為HCl>H2S,
故答案為:HCl>H2S;
(5)電子層結構相同核電荷數越大離子半徑越小,電子層越多離子半徑越大,故離子半徑大小順序是:S 2->Cl->Na+>Al 3+,
故答案為:S 2->Cl->Na+>Al 3+;
(6)Z的最高價氧化物為是Cl2O7,Cl2O7和水反應生成高氯酸,0.25molCl2O7和水反應放出QkJ熱量,則1molCl2O7和水反應放出4QkJ熱量,所以其熱化學反應方程式為:Cl2O7(l)+H2O(l)=2HClO4(aq)△H=-4QkJ/mol,
故答案為:Cl2O7(l)+H2O(l)=2HClO4(aq)△H=-4QkJ/mol.
點評 本題考查結構性質位置關系應用,為高頻考點,側重于學生的分析能力的考查,涉及電子式、半徑比較、熱化學方程式書寫等,正確推斷元素是解本題關鍵,注意掌握微粒半徑大小的比較方法.


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 實現化石燃料清潔利用,就無需開發新能源 | |
| B. | 垃圾是放錯地方的資源,應分類回收利用 | |
| C. | 綠色化學的核心是應用化學原理對環境污染進行治理 | |
| D. | 為提高農作物的產量和質量,應大量使用化肥和農藥 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醋酸溶液能使紫色石蕊溶液變紅 | |
| B. | 醋酸溶液能與碳酸鈉反應產生二氧化碳氣體 | |
| C. | 煮沸醋酸溶液再冷卻到常溫,發現溶液pH變大 | |
| D. | 濃度均為1mol/L的鹽酸和醋酸,前者導電能力強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題

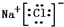 、
、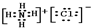
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 逐漸增大 | B. | 逐漸減小 | ||
| C. | 先逐漸增大后減小 | D. | 先逐漸減小后增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com