
分析 (1)氰化鈉為強堿弱酸鹽,水解生成氫氰酸和氫氧化鈉,溶液呈堿性;
(2)①使濕潤的紅色石蕊試紙變藍的氣體為氨氣,根據原子守恒,同時生成碳酸氫鈉;
②根據原子守恒和電荷守恒解答;
(3)①非金屬性強的元素顯示負價,非金屬性弱的則顯示正價;
②根據信息:CN-能夠被氧氣氧化成HCO3-,同時生成NH3來書寫方程式;
③A.該電解質溶液呈堿性,電解時,用不活潑金屬或導電非金屬作陽極,可以用較活潑金屬作陰極;
B.陽極上氯離子失電子生成氯氣,氯氣和氫氧根離子反應生成次氯酸根離子和水;
C.陰極上水失電子生成氫氣和氫氧根離子;
D.陽極產生的ClO-將CN-氧化為兩種無污染的氣體,該反應在堿性條件下進行,所以應該有氫氧根離子生成;
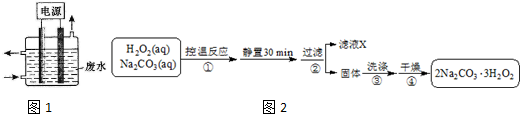
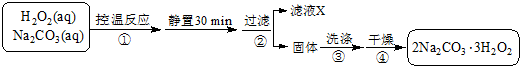
(4)雙氧水和碳酸鈉混合控制溫度發生反應2Na2CO3 (aq)+3H2O2 (aq)?2Na2CO3•3H2O2(s),靜置過濾得到固體2Na2CO3•3H2O2,將固體洗滌、干燥得到較純凈的2Na2CO3•3H2O2.
①過碳酸鈉相當于帶結晶雙氧水的碳酸鈉,具有雙氧水的性質,催化劑、還原性物質易促進過碳酸鈉反應而導致失效;
②先寫出反應的化學方程式,然后根據雙氧水與高錳酸鉀的物質的量關系計算出樣品中雙氧水的百分含量.
解答 解:(1)氰化鈉為強堿弱酸鹽,水解反應為:CN-+H2O?HCN+OH-,溶液呈堿性,故答案為:CN-+H2O?HCN+OH-;
(2)①用雙氧水處理氰化鈉,產生一種能使濕潤的紅色石蕊試紙變藍的氣體為氨氣,根據原子守恒一種酸式鹽為碳酸氫鈉,所以反應為:NaCN+H2O2+H2O═NaHCO3+NH3↑,
故答案為:NaCN+H2O2+H2O═NaHCO3+NH3↑;
②CN-+S2O32-═A+SO32-,根據電荷守恒,A為-1價的陰離子,根據原子守恒,A中含有1個硫原子、1個碳原子、1個氮原子,所以A為:SCN-,
故答案為:SCN-;
(3)①CN-中C元素顯+2價,N元素顯-3價,說明N非金屬性強,故答案為:>;
②CN-能夠被氧氣氧化成HCO3-,同時生成NH3得出方程式為:2CN-+4H2O+O2$\frac{\underline{\;微生物\;}}{\;}$2HCO3-+2NH3,故答案為:2CN-+4H2O+O2$\frac{\underline{\;微生物\;}}{\;}$2HCO3-+2NH3;
③A.該電解質溶液呈堿性,電解時,用不活潑金屬或導電非金屬作陽極,可以用較活潑金屬作陰極,所以可以用石墨作陽極、鐵作陰極,故A正確;
B.陽極上氯離子失電子生成氯氣,氯氣和氫氧根離子反應生成次氯酸根離子和水,所以陽極反應式為Cl-+2OH--2e-═ClO-+H2O,故B正確;
C.電解質溶液呈堿性,則陰極上水失電子生成氫氣和氫氧根離子,電極反應式為2H2O+2e-═H2↑+2OH-,故C正確;
D.陽極產生的ClO-將CN-氧化為兩種無污染的氣體,兩種氣體為二氧化碳和氮氣,該反應在堿性條件下進行,所以應該有氫氧根離子生成,反應方程式為2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH-,故D錯誤;
故答案為:D;
(4)①過碳酸鈉相當于帶結晶雙氧水的碳酸鈉,具有雙氧水的性質,FeCl3能作雙氧水分解的催化劑,KCN具有還原性,能被過碳酸鈉氧化,CuSO4催化雙氧水的分解,硅酸鈉不與過碳酸鈉反應,
故答案為:C;
②高錳酸鉀溶液與過碳酸鈉反應的化學方程式為:6KMnO4+5(2Na2CO3•3H2O2)+19H2SO4═3K2SO4+6MnSO4+10Na2SO4+10CO2↑+15O2↑+34H2O,滴定過程中消耗2.000x10-2 mol•L-1 KMnO4標準溶液的物質的量為:2.000x10-2 mol•L-1×0.03L=6.000x10-4mol,
設過氧化氫的質量為xg,根據關系式
KMnO4~2Na2CO3•3H2O2~15H2O2
6mol 15×34g
6.000x10-4mol x
x=0.051
過氧化氫的質量分數=$\frac{0.051g}{0.2g}$=25.50%
故答案為:25.50%.
點評 本題考查了過碳酸鈉的實驗方案、化學方程式書寫、物質質量分數的計算等知識,題目難度較大,注意化學實驗原理,能夠根據反應方程式進行簡單的化學計算,試題培養了學生的分析、理解能力及靈活應用所學知識的能力.


 出彩同步大試卷系列答案
出彩同步大試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,16 gO2中含有的氧分子數為NA | |
| B. | 1 molOH-中含有的電子數為10NA | |
| C. | 標準狀況下,11.2 L H2O中含有的氫原子數為NA | |
| D. | 1 mol/LBaCl2溶液中含有的鋇離子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NiOOH | B. | Ni(OH)2 | C. | Cd | D. | Cd(OH)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 9.02g | B. | 8.26g | C. | 8.61g | D. | 7.04g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 純凈物都是由同種分子構成 | |
| B. | 純凈物可能是單質,也可能是化合物 | |
| C. | 礦泉水是純凈物 | |
| D. | 純凈物就是由同種元素組成的物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe3+ | B. | Fe2+ | C. | Al3+ | D. | Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com