
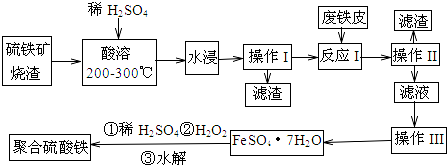
分析 硫鐵礦燒渣(主要成分是Fe3O4、Fe2O3、FeO和二氧化硅),加硫酸加熱酸溶,水浸,過濾出不溶于酸的二氧化硅,濾液中含有硫酸鐵和硫酸亞鐵,加廢鐵皮,Fe與三價鐵離子反應生成亞鐵離子,過濾去除多余的鐵,濾液為硫酸亞鐵溶液,然后蒸發濃縮、冷卻結晶,得到硫酸亞鐵晶體,晶體中加稀硫酸、雙氧水得到聚合硫酸鐵,
(1)Fe2+具有還原性,可與KMnO4發生氧化還原反應;
(2)增大燒渣固體與硫酸的接觸的表面積,可加快反應速率;
(3)堿性條件下,有利于油脂的水解;
(4)Fe2O3溶于硫酸生成硫酸鐵和水;
(5)由溶液得到晶體FeSO4•7H2O,需蒸發濃縮、冷卻結晶,洗滌的操作方法是向漏斗里加入蒸餾水,使水面沒過沉淀物,等水自然流完后,重復操作2-3次;
(6)酸性條件下H2O2氧化Fe2+為Fe3+,同時雙氧水被還原生成水.
解答 解:硫鐵礦燒渣(主要成分是Fe3O4、Fe2O3、FeO和二氧化硅),加硫酸加熱酸溶,水浸,過濾出不溶于酸的二氧化硅,濾液中含有硫酸鐵和硫酸亞鐵,加廢鐵皮,Fe與三價鐵離子反應生成亞鐵離子,過濾去除多余的鐵,濾液為硫酸亞鐵溶液,然后蒸發濃縮、冷卻結晶,得到硫酸亞鐵晶體,晶體中加稀硫酸、雙氧水得到聚合硫酸鐵,
(1)“酸溶”后的溶液中含有Fe3+和Fe2+,Fe2+具有還原性,所以檢驗Fe2+試劑是KMnO4 溶液,現象是紫紅色褪去,
故答案為:KMnO4溶液;
(2)硫鐵礦燒渣在“酸溶”前要粉碎的主要目的是增大燒渣固體與硫酸的接觸的表面積,加快燒渣的溶解速率,
故答案為:增大燒渣與硫酸的接觸面積,加快燒渣的溶解;
(3)堿性條件下,有利于油脂的水解,廢鐵皮使用前要用純堿溶液浸泡,目的是洗去鐵表面油污,
故答案為:洗去鐵表面油污;
(4)Fe2O3溶于硫酸生成硫酸鐵和水,反應的化學方程式為:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
故答案為:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(5)操作Ⅲ的目的是由溶液得到晶體FeSO4•7H2O,需蒸發濃縮、冷卻結晶,洗滌的操作方法是向漏斗里加入蒸餾水,使水面沒過沉淀物,等水自然流完后,重復操作2-3次,
故答案為:蒸發濃縮(加熱濃縮)、冷卻結晶;向漏斗里加入蒸餾水,使水沒過沉淀物,等水自然流完后,重復操作2~3次;
(6)酸性條件下H2O2氧化Fe2+為Fe3+,同時雙氧水被還原生成水,其反應的離子方程式為:2Fe2++H2O2+2H+=2Fe3++2H2O;
故答案為:2Fe2++H2O2+2H+=2Fe3++2H2O.
點評 本題考查制備實驗方案的設計與評價,為高頻考點和常見題型,題目難度中等,準確的分析流程、明確鐵及其化合物的性質是解題的關鍵,側重學生分析能力和創新能力的培養.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
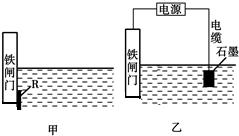 鋼鐵很容易生銹而被腐蝕,每年因腐蝕而損失的鋼鐵占世界鋼鐵年產量的四分之一.
鋼鐵很容易生銹而被腐蝕,每年因腐蝕而損失的鋼鐵占世界鋼鐵年產量的四分之一.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 還原性:Cr3+>Fe2+>SO2 | |
| B. | 氧化性:Cr2O72->SO2>Fe3+ | |
| C. | 足量的SO2也不能使Fe2(SO4)3溶液完全褪去顏色 | |
| D. | Fe2(SO4)3在前一個反應中做氧化劑,后一個反應中做還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
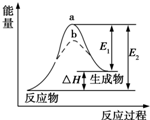
| A. | 如圖可知a一定使用了催化劑 | |
| B. | 該反應為放熱反應,△H=E1-E2 | |
| C. | 使用催化劑,可以改變化學平衡常數 | |
| D. | 使用催化劑,可降低該反應的活化能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 566kJ | B. | 283kJ | C. | 712kJ | D. | 356kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等質量的氫氣完全燃燒分別生成氣態水和液態水,前者△H大于后者 | |
| B. | 破壞反應物全部化學鍵所需要的能量小于破壞生成物全部化學鍵所需要的能量時,該反應為吸熱反應 | |
| C. | 由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1,可知含1molH2SO4的濃硫酸與含1molNaOH的燒堿溶液混合,放出熱量等于57.3kJ | |
| D. | H2的燃燒熱為285.8kJ•mol-1,則氫氣燃燒的熱化學方程式可表示為:H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-285.8kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
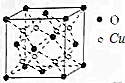 科學家研究發現金屬離子吸收氧氣的能力十分巨大,人體血液中的血紅蛋白依靠亞鐵離子結合氧氣,其他金屬離子(Cu2+、Zn2+等)也可以實現結合和運輸氧氣的目的.最近丹麥科學家研發了一種晶體材料,該晶體吸收氧氣的能力依靠鈷離子,它可以讓人在水下持久地獲得氧氣.
科學家研究發現金屬離子吸收氧氣的能力十分巨大,人體血液中的血紅蛋白依靠亞鐵離子結合氧氣,其他金屬離子(Cu2+、Zn2+等)也可以實現結合和運輸氧氣的目的.最近丹麥科學家研發了一種晶體材料,該晶體吸收氧氣的能力依靠鈷離子,它可以讓人在水下持久地獲得氧氣.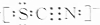 ,則SCN-中σ 鍵與π鍵的個數比為1:1.
,則SCN-中σ 鍵與π鍵的個數比為1:1.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com