
| A. | 一定溫度下,將濃度為0.1 mol•L-1 HF溶液加水不斷稀釋過程中,電離度和Ka(HF)保持不變,$\frac{c({F}^{-})}{c(HF)}$始終保持增大 | |
| B. | 濃度均為0.1mol•L-1的Na2SO3、NaHSO3混合溶液中:3c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3) | |
| C. | 在0.1mol•L-1氨水中滴加0.1mol•L-1鹽酸,恰好完全中和時pH=a,則由水電離產生的c(OH-)=10-amol•L-1 | |
| D. | 已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,則Ag2CrO4的溶解度小于AgCl |
分析 A、弱酸加水稀釋,其電離度增大,電離平衡常數不變,氟離子和氫離子物質的量同等程度的增大;
B、根據溶液中的物料守恒知識來回答;
C、完全中和生成氯化銨,為強酸弱堿鹽,水解呈酸性;
D、根據溶度積可計算溶液的物質的量濃度,根據物質的量濃度可比較.
解答 解:A、將濃度為0.1 mol•L-1 HF溶液加水不斷稀釋過程中,Ka(HF)=c(H+)×$\frac{c({F}^{-})}{c(HF)}$始終保持增大保持不變,氫離子濃度減小,$\frac{c({F}^{-})}{c(HF)}$始終保持增大,電離度增加,故A錯誤;
B、濃度均為0.1mol•L-1的Na2SO3、NaHSO3混合溶液中,存在:2c(Na+)=3[c(SO32-)+c(HSO3-)+c(H2SO3),故B錯誤;
C、在0.1mol•L-1氨水中滴加0.1mol•L-1鹽酸,剛好完全中和時,得到氯化銨溶液pH=a,此時a<7,水的電離受到促進,則溶液中水電離產生的c(OH-)=10-amol•L-1,故C正確;
D、Ksp(Ag2CrO4)=x2×0.5x=0.5x3=2.0×10-12,x3=4.0×10-12,即x═$\root{3}{4×1{0}^{-12}}$,因為AgCl飽和溶液中Ag+的濃度為$\sqrt{1.8×1{0}^{-10}}$,所以溶解度Ag2CrO4>AgCl,故D錯誤.
故選C.
點評 本題考查了溶液pH的計算、溶液中離子濃度大小比較、難溶電解質的沉淀平衡等知識,題目難度中等,注意掌握酸堿混合后溶液的定性判斷及溶液中pH的計算方法,學會利用電荷守恒、物料守恒、鹽的水解原理結合溶液中的電離平衡問題.


科目:高中化學 來源: 題型:選擇題
| A. | 鋅粒與稀硫酸的反應 | |
| B. | 生石灰與水的反應 | |
| C. | 甲烷在空氣中燃燒的反應 | |
| D. | Ba(OH)2•8H2O晶體與NH4Cl晶體的反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Zn2+、Cu2+、Fe3+ | B. | Zn2+、Cu2+、Fe2+ | ||
| C. | Zn2+、Fe2+、Cu2+、Fe3+ | D. | Zn2+、Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5:1 | B. | 4:1 | C. | 3:2 | D. | 1:5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
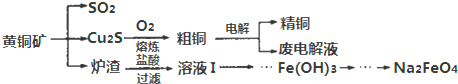
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
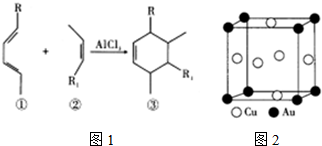
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 晶體類型 | 離子晶體 | 原子晶體 | 分子晶體 |
| 各組中物質的編號 | ①④ | ②⑤ | ③⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題

 .
. .
. 與過量的
與過量的 也可以發生Reformatsky反應,試寫出該生成物的結構簡式
也可以發生Reformatsky反應,試寫出該生成物的結構簡式 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com