
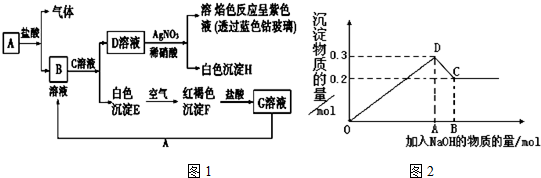
分析 (1)由轉化關系可知,由白色沉淀E在空氣中轉化為紅褐色沉淀F,則E為Fe(OH)2,F為Fe(OH)3,溶液D與硝酸銀溶液得到白色沉淀H,所得溶液焰色反應為紫色,故含有K+,白色沉淀H為AgCl,故D為KCl,由溶液C+溶液B→KCl+Fe(OH)2,為FeCl2與KOH的反應,Fe(OH)3與鹽酸反應得到G,G與A反應得到B,可知B為FeCl2,C為KOH,G為FeCl3,A為Fe,據此解答;
(2)①OD段是:MgCl2與氫氧化鈉反應生成氫氧化鎂沉淀與氯化鈉,AlCl3與氫氧化鈉反應生成氫氧化鋁沉淀與氯化鈉;DC段是氫氧化鋁與氫氧化鈉反應生成偏鋁酸鈉與水;
②由圖可知,沉淀量最大為0.3mol,沉淀量最小為0.2mol,可知氫氧化鎂為0.2mol,氫氧化鋁為0.3mol-0.2mol=0.1mol,根據守恒計算Mg2+、Al3+物質的量濃度之比;
③C點是氫氧化鋁恰好被溶解為偏鋁酸鈉,此時沉淀為氫氧化鎂,根據方程式計算據方程式計算OA段、AB段消耗NaOH物質的量,進而計算加入NaOH物質的量;
④根據③中計算可知OA段、AB段消耗NaOH物質的量之比.
解答 解:(1)由轉化關系可知,由白色沉淀E在空氣中轉化為紅褐色沉淀F,則E為Fe(OH)2,F為Fe(OH)3,溶液D與硝酸銀溶液得到白色沉淀H,所得溶液焰色反應為紫色,故含有K+,白色沉淀H為AgCl,故D為KCl,由溶液C+溶液B→KCl+Fe(OH)2,為FeCl2與KOH的反應,Fe(OH)3與鹽酸反應得到G,G與A反應得到B,可知B為FeCl2,C為KOH,G為FeCl3,A為Fe.
①由上述分析可知,B為KOH,D為KCl,故答案為:KOH;KCl;
②由E轉變成F的化學方程式為:4Fe(OH)2+2H2O+O2=4Fe(OH)3,故答案為:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
③用KSCN鑒別FeCl3現象:溶液變為血紅色;向FeCl3溶液加入Fe的有關離子反應方程式:Fe+2Fe3+=3Fe2+,故答案為:溶液變為血紅色;Fe+2Fe3+=3Fe2+;
(2)①氯化鎂和氯化鋁均可以和氫氧化鈉發生反應,生成沉淀氫氧化鎂和氫氧化鋁,則OD段發生反應的離子方程式Al3++3OH-=Al(OH)3↓、Mg2++2OH-=Mg(OH)2↓;
DC段是氫氧化鋁與氫氧化鈉反應生成偏鋁酸鈉與水,反應離子方程式為Al(OH)3+OH-=AlO2-+2H2O,
故答案為:Al3++3OH-=Al(OH)3↓、Mg2++2OH-=Mg(OH)2↓;Al(OH)3+OH-=AlO2-+2H2O;
②由圖可知,沉淀量最大為0.3mol,沉淀量最小為0.2mol,可知氫氧化鎂為0.2mol,氫氧化鋁為0.3mol-0.2mol=0.1mol,根據守恒可知Mg2+、Al3+物質的量濃度之比為0.2mol:0.1mol=2:1,
故答案為:2:1;
③C點是氫氧化鋁恰好被溶解為偏鋁酸鈉,此時沉淀為氫氧化鎂,Al3+已經轉化為AlO2-,Mg2+已經轉化為Mg(OH)2,
氫氧化鎂為0.2mol,氫氧化鋁為0.3mol-0.2mol=0.1mol,由Al3++3OH-=Al(OH)3↓、Mg2++2OH-=Mg(OH)2↓,可知OA段消耗NaOH為0.1mol×3+0.2mol×2=0.7mol,由Al(OH)3+OH-=AlO2-+2H2O可知,AB段消耗NaOH為0.1mol,故C點加入NaOH為0.7mol+0.1mol=0.8mol,
故答案為:0.8;AlO2-;Mg(OH)2;
④根據③中計算可知OA段、AB段消耗NaOH物質的量之比0.7mol:0.1mol=7:1,故答案為:7:1.
點評 本題考查無機物推斷、混合物有關計算,屬于拼合型題目,(1)中物質顏色及焰色反應為推斷突破口,(2)中關鍵是明確各階段發生的反應,難度中等.


科目:高中化學 來源: 題型:解答題
 小蘇打(NaHCO3)試樣中含有碳酸鈉晶體(Na2CO3•10H2O),為測定試樣中小蘇打的質量分數w(NaHCO3),實驗小組同學設計了如下裝置進行實驗.
小蘇打(NaHCO3)試樣中含有碳酸鈉晶體(Na2CO3•10H2O),為測定試樣中小蘇打的質量分數w(NaHCO3),實驗小組同學設計了如下裝置進行實驗.| 序號 | a | b | c | d | e |
| 數據 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m2、m5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO42-、CO32-、F- | B. | CO32-、SO42-、F- | C. | CO32-、F-、SO42- | D. | F-、CO32-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗后剩余的鈉粒可放回原試劑瓶中 | |
| B. | 剛剛切開的鈉的銀白色斷面會很快變暗 | |
| C. | 自然界中無游離態的鈉存在 | |
| D. | 鈉在空氣中加熱時生成白色的過氧化鈉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在稀硫酸中加入銅粉,銅粉不溶解,再加入Cu(NO3)2固體,銅粉仍不溶解 | |
| B. | 某氣體能使濕潤的紅色石蕊試紙變藍,該氣體的水溶液一定顯堿性 | |
| C. | 濃硝酸與木炭反應的離子方程式:C+4H++4NO3-=CO2↑+4NO2↑+2H2O | |
| D. | HNO3→NO→NO2,以上各步變化均能通過一步實現 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com