
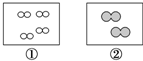
 如圖所示,①和②為兩個體積相同的固定容器,圖中“○”和“●”分別表示氫原子和氧原子,則下列說法正確的是( )
如圖所示,①和②為兩個體積相同的固定容器,圖中“○”和“●”分別表示氫原子和氧原子,則下列說法正確的是( )| A. | 若①中的H2為1 mol,則②中所含原子總數為3.01×1023個 | |
| B. | ①和②中氣體的質量之比為1:8 | |
| C. | H2、O2均能發生化合反應,但不能發生置換反應 | |
| D. | 兩容器的溫度和壓強均相同 |
分析 A.若①中的H2為1 mol,則②中所含氧氣分子為0.5mol;
B.氣體分子數之比等于其物質的量之比,結合摩爾質量計算質量之比;
C.氫氣還原氧化銅發生置換反應,氧氣氧化硫化氫生成單質硫發生置換反應;
D.①和②為兩個體積相同的固定容器,但分子個數不同,所以溫度和壓強不可能均相同;
解答 解:A.若①中的H2為1 mol,則②中所含氧氣分子為0.5mol,原子總數為6.02×1023個,故A錯誤;
B.若①中的H2為1 mol,則②中所含氧氣分子為0.5mol,①和②中氣體的質量之比為1×2:0.5×32=1:8,故B正確;
C.氫氣還原氧化銅發生置換反應,H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,氧氣氧化硫化氫生成單質硫發生置換反應,O2+2H2S=2S+2H2O,H2、O2均能發生化合反應,都能發生置換反應,故C錯誤;
D.兩容器的體積相同,但分子個數不同,所以兩容器的溫度和壓強不可能均相同,故D錯誤;
故選B.
點評 本題考查了阿伏伽德羅常定律、氣體物質的量和微粒數、質量的計算分析判斷,掌握基礎是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
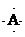 ,B原子L層的電子總數是K層的3倍;0.1mol C單質能從酸中置換出2.24L氫氣(標準狀況),同時它的電子層結構變得與氖原子的電子層結構相同;D離子的半徑比C離子的小,D離子與B離子的電子層結構相同.
,B原子L層的電子總數是K層的3倍;0.1mol C單質能從酸中置換出2.24L氫氣(標準狀況),同時它的電子層結構變得與氖原子的電子層結構相同;D離子的半徑比C離子的小,D離子與B離子的電子層結構相同.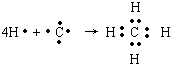 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
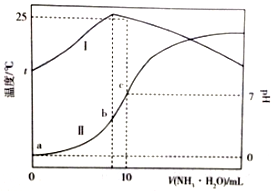 溫度為t℃時,在10mL1.0mol/L的鹽酸中,逐滴滴入xmol/L的氨水,隨著氨水遂漸加入,溶液中的溫度變化曲線(曲線I)和pH變化曲線(曲線II)如圖所示(忽略混合時溶液體積的變化).下列有關判斷正確的是( )
溫度為t℃時,在10mL1.0mol/L的鹽酸中,逐滴滴入xmol/L的氨水,隨著氨水遂漸加入,溶液中的溫度變化曲線(曲線I)和pH變化曲線(曲線II)如圖所示(忽略混合時溶液體積的變化).下列有關判斷正確的是( )| A. | c點時,c(NH3•H2O)=1.0mol•L-1 | B. | a點時,水的電離程度最大 | ||
| C. | b點時,c(NH4+)>c(Cl-)>c(H+)>c(OH-) | D. | c點時,c(NH3•H2O)=$\frac{x-1}{2}$mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化合反應 | B. | 復分解反應 | C. | 置換反應 | D. | 分解反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{vn}{22.4}$ | B. | $\frac{22.4n}{v}$ | C. | $\frac{vn}{5.6}$ | D. | $\frac{22.4n}{3v}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
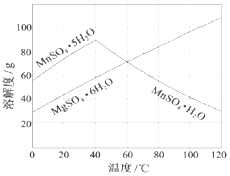 軟錳礦(主要成分MnO2,雜質金屬元素Fe、Al、Mg等)的水懸濁液與煙氣中SO2反應可制備MnSO4•H2O,反應的化學方程式為:MnO2+SO2=MnSO4
軟錳礦(主要成分MnO2,雜質金屬元素Fe、Al、Mg等)的水懸濁液與煙氣中SO2反應可制備MnSO4•H2O,反應的化學方程式為:MnO2+SO2=MnSO4查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com