

分析 孔雀石的主要成分為Cu2(OH)2CO3,還含少量FeCO3、Si的化合物,加入稀硫酸反應后生成二氧化碳氣體,過濾得到二氧化硅固體,得到濾液1為硫酸銅、硫酸亞鐵溶液,“除雜”時先通入足量過氧化氫將Fe2+氧化成Fe3+,得到溶液2為硫酸銅、硫酸鐵溶液,再加入CuO固體調節溶液pH,沉淀鐵離子生成氫氧化鐵沉淀;過濾得到濾液為硫酸銅溶液,濾液3為硫酸銅溶液,通過蒸發濃縮,冷卻結晶,過濾洗滌得到硫酸銅晶體;
(1)孔雀石的主要成分為Cu2(OH)2CO3,還含少量FeCO3、Si的化合物,步驟Ⅰ中涉及的反應是Cu2(OH)2CO3和FeCO3與硫酸發生復分解反應生成二氧化碳,
(2)步驟Ⅱ中加入試劑①的目的是氧化亞鐵離子為鐵離子,便于除去,所加試劑能和亞鐵離子反應且不能引入新的雜質;
(3)步驟Ⅲ加入CuO目的是調節溶液的PH使鐵離子全部沉淀;
(4)溶液中得到溶質的方法是蒸發濃縮冷卻結晶、過濾洗滌;
(5)孔雀石與焦炭一起加熱可以生成Cu、二氧化碳和水,依據原子守恒配平書寫化學方程式;
(6)稱量粉末的質量為1.6g為硫酸銅質量,受熱前后質量變化為結晶水的質量,結合化學方程式CuSO4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+xH2O計算x.
解答 解:孔雀石的主要成分為Cu2(OH)2CO3,還含少量FeCO3、Si的化合物,加入稀硫酸反應后生成二氧化碳氣體,過濾得到二氧化硅固體,得到濾液1為硫酸銅、硫酸亞鐵溶液,“除雜”時先通入足量過氧化氫將Fe2+氧化成Fe3+,得到溶液2為硫酸銅、硫酸鐵溶液,再加入CuO固體調節溶液pH,沉淀鐵離子生成氫氧化鐵沉淀;過濾得到濾液為硫酸銅溶液,濾液3為硫酸銅溶液,通過蒸發濃縮,冷卻結晶,過濾洗滌得到硫酸銅晶體;
(1)孔雀石的主要成分為Cu2(OH)2CO3,還含少量FeCO3、Si的化合物,步驟Ⅰ中涉及的反應是Cu2(OH)2CO3和FeCO3與硫酸發生復分解反應生成二氧化碳,反應的化學方程式為:Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O,FeCO3+2H+=Fe2++CO2↑+H2O;
故答案為:Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O,FeCO3+2H+=Fe2++CO2↑+H2O;
(2)步驟Ⅱ中加入試劑①的目的是氧化亞鐵離子為鐵離子,便于沉淀除去,所加試劑能和亞鐵離子反應且不能引入新的雜質,
a.KMnO4溶液加入后,能氧化亞鐵離子,但會引入鉀離子、錳離子,故a不符合;
b.加入H2O2會氧化亞鐵離子為鐵離子,過氧化氫被還原為水,不引入雜質,故b符合;
c.Fe粉不能氧化亞鐵離子,故c不符合;
d.加入KSCN溶液結合鐵離子形成絡合物,不能氧化亞鐵離子,亞鐵離子的存在會干擾硫酸銅晶體的析出,故d不符合;
故答案為:b;
(3)步驟Ⅲ加入CuO目的是和酸反應,調節溶液的PH使鐵離子全部沉淀,故答案為:消耗酸使溶液pH升高,便于Fe3+形成沉淀除去;
(4)操作Ⅳ是溶液中得到溶質的方法是蒸發濃縮、冷卻結晶、過濾洗滌;
故答案為:加熱濃縮;冷卻結晶;
(5)孔雀石與焦炭一起加熱可以生成Cu、二氧化碳和水,依據原子守恒配平書寫得到的化學方程式為:Cu2(OH)2CO3+C$\frac{\underline{\;\;△\;\;}}{\;}$ 2Cu+2CO2↑+H2O;
故答案為:Cu2(OH)2CO3+C$\frac{\underline{\;\;△\;\;}}{\;}$ 2Cu+2CO2↑+H2O;
(6)稱取2.4g硫酸銅晶體,加熱至質量不再改變時,稱量粉末的質量為1.6g為硫酸銅質量,n(CuSO4)物質的量=$\frac{1.6g}{160g/mol}$=0.01mol,受熱質量減少2.4g-1.6g=0.8g,水的物質的量=$\frac{0.8g}{18g/mol}$=0.044mol;
CuSO4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+xH2O
1 x
0.01mol 0.044mol
x=4.4
故答案為:4.4.
點評 本題考查了物質分離方法和提純的應用,主要是物質性質的理解應用,掌握實驗基本操作和流程分析是關鍵,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | X3Y2 | B. | X2Y | C. | Y3X2 | D. | Y2X3 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 在標準狀態下,1L庚烷完全燃燒后,所生成的氣態產物的分子數為$\frac{7}{22.4}$NA | |
| B. | 1mol碳正離子CH5+所含的電子數為10NA | |
| C. | 標準狀態下,16g甲烷完全燃燒所消耗的氧氣的分子數為2NA | |
| D. | 0.5mol C3H8分子中含C-H共價鍵2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
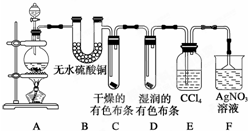 某校化學實驗興趣小組為了探究在實驗室制備Cl2的過程中有水蒸氣和HCl揮發出來,同時探究氯氣的漂白原理,甲同學設計了如圖所示的實驗裝置(支撐用的鐵架臺省略),按要求回答問題.
某校化學實驗興趣小組為了探究在實驗室制備Cl2的過程中有水蒸氣和HCl揮發出來,同時探究氯氣的漂白原理,甲同學設計了如圖所示的實驗裝置(支撐用的鐵架臺省略),按要求回答問題.查看答案和解析>>
科目:高中化學 來源: 題型:解答題


| 實驗操作 | 主要現象 | 結論或解釋 |
| 步驟1:取少量固體于試管中,加入足量 ①氯化鐵溶液. | 固體減少且剩余, 淡黃色溶液變淺. | 固體中含有金屬鐵 |
| 步驟2:分離步驟1的剩余固體于另一試管中,加入足量 ②鹽酸,將反應后溶液分成甲、乙兩份. | 固體全部消失. | 反應的化學方程式 ③ Fe3O4+8HCl=FeCl2+2FeCl3+H2O. |
| 步驟3:在步驟2的甲溶液中加入幾滴 ④高錳酸鉀溶液. | 紫紅色褪去. | 溶液中含有Fe2+. |
| 步驟4:在步驟2的乙溶液中加入幾滴⑤KSCN溶液. | 溶液變成紅色. | 溶液中含有Fe3+. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaOH溶液 | B. | 氨水 | C. | KMnO4,ZnCO3 | D. | H2O2,ZnO |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 9.0 | B. | 9.5 | C. | 1 0.5 | D. | 1 1.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②④ | B. | ②④ | C. | ②③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加熱飽和三氯化鐵溶液制備氫氧化鐵膠體:Fe3++3H2O$\stackrel{△}{?}$Fe(OH)3(膠體)+3H+ | |
| B. | 磷酸二氫根電離的離子方程式:H2PO4-+H2O?H3O++HPO42- | |
| C. | 少量碳酸氫鈣溶液與氫氧化鈉溶液混合的離子方程式Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- | |
| D. | 在0.5mol•L-1的K2Cr2O7溶液中存在如下平衡:CrO72-+H2O?2CrO42-+2H+,其平衡常數K的表達式為K=$\frac{{c}^{2}(Cr{O}_{4}^{2-})•{c}^{2}({H}^{+})}{c(C{r}_{2}{O}_{7}^{2-})}$ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com