
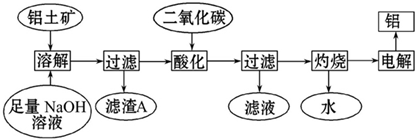
分析 鋁土礦的主要成分是Al2O3,另外含有的少量SiO2均能溶解于過量NaOH溶液,過濾除去其中不溶于NaOH的Fe2O3等雜質及生成的Na2Al2Si2O8,所得濾液為NaAlO2及過量NaOH的溶液,通入過量CO2可得到Al(OH)3沉淀,過濾、洗滌再加熱分解可得到Al2O3,最后電解氧化鋁可得到鋁,
(1)氧化鋁、二氧化硅與NaOH溶液反應均生成鹽和水;
(2)只有氧化鐵與堿不反應,結合信息②可知還生成Na2Al2Si2O8,氧化鐵用于冶煉鐵,過濾利用玻璃棒引流;
(3)第三步中,選用二氧化碳作酸化劑,可將Al元素全部轉化為沉淀;
(4)根據Al的化學性質及不生成有毒氣體來解答.
解答 解:(1)氧化鋁、二氧化硅與NaOH溶液反應均生成鹽和水,離子反應分別為Al2O3+2OH-═2AlO2-+H2O、SiO2+2OH-═SiO32-+H2O,
故答案為:Al2O3+2OH-═2AlO2-+H2O;SiO2+2OH-═SiO32-+H2O;
(2)只有氧化鐵與堿不反應,結合信息②可知還生成Na2Al2Si2O8,則濾渣A的主要成分為Fe2O3、Na2Al2Si2O8,氧化鐵用于冶煉鐵,過濾利用玻璃棒引流,
故答案為:Fe2O3、Na2Al2Si2O8;作煉鐵的原料(或作生產硅酸鹽產品的原料);引流;
(3)經過足量氫氧化鈉溶液的溶解,大部分鋁元素均以NaAlO2的形式存在于濾液中,通入過量二氧化碳可以將NaAlO2完全轉化為Al(OH)3,所以第三步中,選用二氧化碳作酸化劑的原因為將NaAlO2完全轉化為Al(OH)3,故答案為:將NaAlO2完全轉化為Al(OH)3;
(4)因鋁與濃硫酸在常溫下發生鈍化,加熱溶解會產生有毒氣體SO2,原料利用率低;稀硝酸能溶解鋁但會產生NO氣體,污染空氣,硝酸利用率低;而鋁與稀硫酸反應速率較快,產生的H2對空氣無污染,則選稀硫酸溶解Al最好,
故答案為:B.
點評 本題考查Al的化學性質,注意把握流程中發生的化學反應為解答的關鍵,注重信息與所學知識的結合分析解決問題,側重知識遷移應用能力的考查,題目難度中等.


 同步練習河南大學出版社系列答案
同步練習河南大學出版社系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 操 作 | 現 象 |
| 點燃酒精燈,加熱至170℃ | Ⅰ:A中燒瓶內液體漸漸變黑 Ⅱ:B內氣泡連續冒出,溶液逐漸褪色 |
| … | |
| 實驗完畢,清洗燒瓶 | Ⅲ:A中燒瓶內附著少量黑色顆粒狀物,有刺激性氣味逸出 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
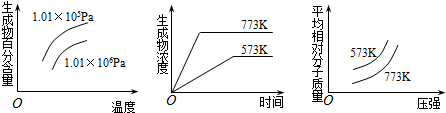
| A. | N2(g)+3H2(g)?2NH3(g) (正反應為放熱反應) | |
| B. | 2SO3(g)?2SO2(g)+O2(g) (正反應為吸熱反應) | |
| C. | 4NH3(g)+5O2(g)?4NO+6H2O(g) (正反應為放熱反應) | |
| D. | 2HI(g)?I2(g)+H2(g) (正反應為吸熱反應) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com