
| 操 作 | 現 象 |
| 點燃酒精燈,加熱至170℃ | Ⅰ:A中燒瓶內液體漸漸變黑 Ⅱ:B內氣泡連續冒出,溶液逐漸褪色 |
| … | |
| 實驗完畢,清洗燒瓶 | Ⅲ:A中燒瓶內附著少量黑色顆粒狀物,有刺激性氣味逸出 |

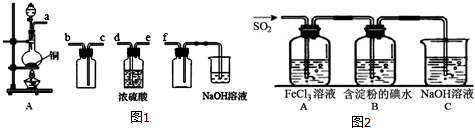
分析 (1)根據儀器①②的構造寫出儀器①②的名稱;
(2)a.乙烯分子中含有碳碳雙鍵,能夠與溴的四氯化碳發生加成反應生成1,2-二溴乙烷;
b.SO2能和溴水發生氧化還原反應;
(3)二氧化硫的檢驗用品紅溶液,乙烯的檢驗用高錳酸鉀酸性溶液,乙烯和二氧化硫都能使高錳酸鉀酸性溶液褪色,所以先檢驗二氧化硫,然后檢驗乙烯,同在檢驗乙烯之前用NaOH溶液除去SO2,再通過品紅溶液不褪色確認SO2已除干凈,最后用高錳酸鉀酸性溶液褪色檢驗乙烯;
(4)二氧化硫使品紅溶液褪色,也能是使高錳酸鉀酸性溶液褪色;
(5)通過品紅溶液不褪色確認SO2已除干凈,再用高錳酸鉀酸性溶液褪色檢驗乙烯.
解答 解:(1)圖1中儀器①用于測量反應溫度,名稱為溫度計;儀器②由于盛放乙醇和濃硫酸的混合液,名稱為圓底燒瓶,
故答案為:溫度計;圓底燒瓶;
(2)a.向溴的四氯化碳溶液中通入乙烯,乙烯與溴發生加成反應生成1,2-二溴乙烷,所以溶液的顏色很快褪去,反應的方程式為CH2=CH2+Br2→CH2BrCH2Br,
故答案為:CH2=CH2+Br2→CH2BrCH2Br;加成反應;
b.SO2 使溶液褪色的反應方程式,SO2+Br2+2H2O=2H2SO4+2HBr,
故答案為:SO2+Br2+2H2O=2H2SO4+2HBr;
(3)因裝置①用來檢驗SO2,試管中品紅溶液褪色,說明含有SO2,裝置②試管裝有NaOH溶液除去SO2,裝置③試管通過品紅溶液不褪色確認SO2已除干凈,裝置④通過高錳酸鉀酸性溶液褪色檢驗乙烯,
故答案為:①A;②B;③A;④D;
(4)裝置①用來檢驗SO2,試管中品紅溶液褪色,說明含有SO2,裝置②試管裝有NaOH溶液除去混合氣體中的SO2,避免干擾實驗結果,
故答案為:裝置①品紅溶液褪色;除去混合氣體中的SO2,避免干擾實驗結果;
(5)裝置③試管通過品紅溶液不褪色,裝置④通過高錳酸鉀酸性溶液褪色檢驗乙烯,
故答案為:裝置③中品紅溶液不褪色,裝置④高錳酸鉀酸性溶液褪色.
點評 本題主要考查了乙烯的實驗室制法,實驗室制乙烯產物的檢驗,當有多種產物需檢驗時,應考慮先后順序,在除去雜質氣體時不能引入新雜質,題目難度中等,注意掌握常見儀器的干燥及使用方法,明確乙烯的實驗室制法、性質及反應原理.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 0.5molH2O含有的原子數目為1.5NA | B. | 0.5molNH3含有的電子數目為4NA | ||
| C. | 28gCO含有的分子數目為NA | D. | 2NA個氯氣分子的物質的量是2mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+242kJ•mol-1 | B. | 2H2(g)+O2(g)=2H2O(l)△H=+484kJ•mol-1 | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-242kJ•mol-1 | D. | 2H2(g)+O2(g)=2H2O(g)△H=-484kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ⅰ和Ⅱ兩途徑最終達到平衡時,系統內混合氣體的平均相對分子質量不同 | |
| B. | Ⅰ和Ⅱ兩途徑最終達到平衡時,系統內混合氣體的百分組成不同 | |
| C. | 達到平衡時Ⅰ途徑的VA等于Ⅱ途徑的VA | |
| D. | 達到平衡后,第Ⅰ途徑混合氣密度為第Ⅱ途徑混合氣密度的$\frac{1}{2}$ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com