
【題目】已知,常溫下H2S、H2CO3 的電離常數如下表
Ka1 | Ka2 | |
H2S | 9.1×10-8 | 1×10-15 |
H2CO3 | 4.3×10-7 | 5.6×10-11 |
(1)①常溫下,0.1mol/L的硫化鈉溶液和0.1mol.L-1的碳酸鈉溶液,堿性更強的是_______。其原因是_____________________________。
② 常溫下,硫化鈉水解的離子方程式_____________________________。
(2)H2S能與許多金屬離子發生反應,生成溶解度不同和各種顏色的金屬硫化物沉淀,可用于分離和鑒定金屬離子。
①常溫下,NaHS溶液顯______(選填“酸性”、“中性”或“堿性”)
②常溫下,向100 mL 0.1 mol·L-1 H2S溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH與NaOH溶液體積的關系曲線如圖所示:

試分析圖中a、b、c、d四個點,水的電離程度最大的是________;在b點,溶液中各離子濃度由大到小的排列順序是______________________________。
(3)脫除天然氣中的硫化氫既能減少環境污染,又可回收硫資源,該部分硫化氫用過量NaOH溶液吸收后,再以石墨作電極電解該溶液可回收硫,寫出電解得到硫的總反應方程式(忽略氧的氧化還原)_______________;從整個生產工藝的角度分析,該方法不僅能減少環境污染、回收硫、得到一定量的副產物,還具有的優點是___________。
【答案】 硫化鈉溶液 硫化氫的Ka2 小于碳酸的Ka2 ,硫化鈉更易水解 S2- + H2O![]() HS- + OH-、HS- + H2O
HS- + OH-、HS- + H2O![]() H2S + OH- 堿性 c c(Na+)>c(HS-)>c(OH-)=c(H+) >c(S2-) Na2S+2H2O
H2S + OH- 堿性 c c(Na+)>c(HS-)>c(OH-)=c(H+) >c(S2-) Na2S+2H2O![]() S↓+H2↑+2NaOH 或S2-+2H2O
S↓+H2↑+2NaOH 或S2-+2H2O![]() S↓+H2↑+2OH- 產物NaOH可循環使用
S↓+H2↑+2OH- 產物NaOH可循環使用
【解析】試題分析:(1)① H2CO3的第二步電離平衡常數是5.6×10-11,大于H2S的第二步電離平衡常數1×10-15,說明S2-的水解程度大于CO32-;②S2-的水解分兩步進行;(1)①根據HS-的 水解平衡常數和電離平衡常數分析NaHS溶液的酸堿性;②H2S抑制水電離,加入NaOH中和H2S,H2S抑制作用逐漸減小,到c點H2S恰好與NaOH生成Na2S, Na2S水解促進水電離;d點氫氧化鈉過量,過量的氫氧化鈉抑制水電離。NaHS溶液呈堿性,在b點溶液呈中性,所以b點溶質是NaHS和H2S,HS-要水解和電離,HS-、H2S的電離生成 S2-;HS-、H2S、H2O電離出H+。(3)硫化氫用過量NaOH溶液吸收后生成Na2S,電解硫化鈉溶液生成硫、氫氣、氫氧化鈉。
解析:(1)① H2CO3的第二步電離平衡常數是5.6×10-11,大于H2S的第二步電離平衡常數1×10-15,說明S2-的水解程度大于CO32-,硫化鈉更易水解,所以硫化鈉溶液的堿性強;②S2-的水解分兩步進行,硫化鈉水解的離子方程式S2- + H2O![]() HS- + OH-、HS- + H2O
HS- + OH-、HS- + H2O![]() H2S + OH-;(2)①HS-的水解平衡常數
H2S + OH-;(2)①HS-的水解平衡常數 ![]() ,電離平衡常數1×10-15,水解大于電離,所以 NaHS溶液的呈堿性;②H2S抑制水電離,加入NaOH中和H2S,H2S抑制作用逐漸減小,到c點H2S恰好與NaOH生成Na2S, Na2S水解促進水電離;d點氫氧化鈉過量,過量的氫氧化鈉抑制水電離,所以C點水電離程度最大。NaHS溶液呈堿性,在b點溶液呈中性,所以b點溶質是NaHS和H2S, HS-、H2S的電離生成 S2-;HS-、H2S、H2O電離出H+,所以b點,溶液中各離子濃度由大到小的排列順序是c(Na+)>c(HS-)>c(OH-)=c(H+) >c(S2-)。(3)硫化氫用過量NaOH溶液吸收后生成Na2S,電解硫化鈉溶液生成硫、氫氣、氫氧化鈉,電解總方程式為Na2S+2H2O
,電離平衡常數1×10-15,水解大于電離,所以 NaHS溶液的呈堿性;②H2S抑制水電離,加入NaOH中和H2S,H2S抑制作用逐漸減小,到c點H2S恰好與NaOH生成Na2S, Na2S水解促進水電離;d點氫氧化鈉過量,過量的氫氧化鈉抑制水電離,所以C點水電離程度最大。NaHS溶液呈堿性,在b點溶液呈中性,所以b點溶質是NaHS和H2S, HS-、H2S的電離生成 S2-;HS-、H2S、H2O電離出H+,所以b點,溶液中各離子濃度由大到小的排列順序是c(Na+)>c(HS-)>c(OH-)=c(H+) >c(S2-)。(3)硫化氫用過量NaOH溶液吸收后生成Na2S,電解硫化鈉溶液生成硫、氫氣、氫氧化鈉,電解總方程式為Na2S+2H2O![]() S↓+H2↑+2NaOH。該方法不僅能減少環境污染、回收硫、得到一定量的副產物,還具有的優點是NaOH可循環使用。
S↓+H2↑+2NaOH。該方法不僅能減少環境污染、回收硫、得到一定量的副產物,還具有的優點是NaOH可循環使用。
電解:向酸溶液中逐滴加入堿溶液,水電離程度逐漸增大,堿過量時水的電離程度再逐漸減小。NaHA溶液的酸堿性要根據HA-的電離和水解程度判斷,若電離程度大于水解程度,溶液呈酸性;若水解大于電離,則溶液呈性。


科目:高中化學 來源: 題型:
【題目】用以下三種途徑來制取等質量的硝酸銅.
①銅與稀硝酸反應;②銅與濃硝酸反應;③銅先與氧氣反應生成氧化銅,氧化銅再跟硝酸反應.
以下敘述不正確的是( )
A.三種途徑所消耗的銅的質量相等
B.所消耗的硝酸的物質的量是①>②>③
C.途徑③的制備方法是最符合“綠色化學”理念的
D.途徑①中被氧化的銅與被還原的硝酸的物質的量比是3:2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[物質結構與性質]2016年9月南開大學學者首次測試了一種新型鋅離子電池,該電池以Zn(CF3SO3)2為電解質,用有陽離子型缺陷的ZnMn2O4為電極,成功的獲得了穩定的大功率電流。
(1)寫出Mn原子基態核外電子排布式 。
(2)CF3SO3H是一種有機強酸,結構式如圖1所示,通常用 CS2、IF5、H2O2等為主要原料制取。
①1molCF3SO3H分子中含有的σ鍵的數目為 mol。
②H2O2分子中O原子的雜化方式為 。與CS2互為等電子體的分子為 。
③IF5遇水完全水解生成兩種酸,寫出相關化學方程式: 。
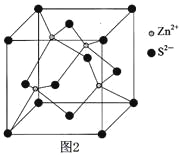
(3)硫化鋅晶體的構型有多種,其中一種硫化鋅的晶胞如圖2,該晶胞中S2-的配位數為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子在指定溶液中一定能大量共存的是( )
A. 純堿溶液中:Al3+、Ba2+、Cl-、NO3-
B. 室溫下,pH=1的溶液中:K+、Fe2+、MnO4-、I-
C. 能使甲基橙變為黃色的溶液中:Na+、Al3+、Cl-
D. 室溫下,![]() =1×10-12的溶液中:K+、Na+、CO32-、NO3-
=1×10-12的溶液中:K+、Na+、CO32-、NO3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2Zn(OH)2·ZnCO3是制備活性ZnO的中間體,以鋅焙砂(主要成分為ZnO,含少量Cu2+、Mn2+等離子)為原料制備2Zn(OH)2·ZnCO3的工藝流程如下:

(1)用(NH4)2SO4與NH3·H2O物質的量之比為1∶2的混合溶液浸取鋅焙砂時,生成[Zn(NH3)4]2+,該反應的離子方程式是 。浸取過程加入H2O2的目的是 。
(2)適量S2-能將Cu2+等離子轉化為硫化物沉淀而除去,若選擇置換的方法除雜,則應加入的物質為 。
(3)氣體A的化學式是 。
(4)過濾3所得濾液可循環使用,其主要成分的化學式是 。證明2Zn(OH)2·ZnCO3沉淀洗滌完全的方法是 。
(5)為實現循環生產,下列物質中可以用來代替(NH4)2S完成除雜的是 。(填字母)
a.Na2S b.K2S c.BaS
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上利用H2SiF6溶液制備BaF2,同時可得到副產品SiO2,其工藝如下:

已知:焙燒過程的反應為(NH4)2SiF6+ BaCO3![]() BaSiF6+ 2NH3↑+ CO2↑+H2O↑
BaSiF6+ 2NH3↑+ CO2↑+H2O↑
(1)焙燒的氣體產物能恰好完全反應生成物質A,則A的化學式為 。
(2)氨解反應為放熱反應,且反應能進行完全。該反應需降溫冷卻的原因為 、 。
(3)熱解的另一產物是含兩種元素的氣體,該氣體水解的化學方程式是 。
(4)SiO2可用于制作 ,該物質在信息傳輸中具有重要應用。
(5)為保持該過程的持續循環,每生成1 mol BaF2,理論上需補充原料H2SiF6 mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了測定草酸晶體H2C2O4·xH2O中的x值,某實驗小組進行實驗,步驟如下:
①稱取1.260g草酸晶體,配成100mL溶液。
②取25.00mL該H2C2O4溶液加入錐形瓶內,再加入適量稀硫酸。
③用濃度為0.1000mol/L的KMnO4溶液滴定H2C2O4溶液,當_______時,滴定結束。
④記錄數據,重復實驗。整理數據如下:
實驗序號 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列問題:
(1)步驟①需要使用燒杯、量筒、玻璃棒,還缺少的玻璃儀器為_______(填名稱);步驟③滴定過程中,盛裝KMnO4溶液的儀器為__________________(填名稱)。
(2)該反應原理的離子方程式為___________________________________;
(3)請將步驟③補充完整_________________________________________;
(4)根據數據,計算H2C2O4溶液的物質的量濃度為______mol/L,x=____________;
(5)若滴定終點讀數時俯視液面,則x值會________(填“偏大”、“偏小”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學在實驗報告中記錄下列數據,其中正確的是
A. 用 25mL 量筒量取 12.36mL 鹽酸
B. 用托盤天平稱量 8.75g 食鹽
C. 用 500mL 的容量瓶配制 450mL 溶液
D. 用 50mL 蒸餾燒瓶盛裝 40mL 溶液進行蒸餾實驗
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com