
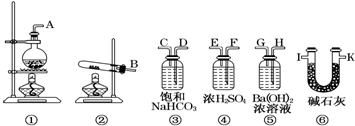
分析 根據裝置圖可知,為測定樣品中Na2CO3的質量分數,先將樣品在試管中加熱,將生成氣體通往氫氧化鋇溶液中,根據氫氧化鋇溶液質量的質量的增加可知二氧化碳的質量,根據二氧化碳的質量可知樣品中碳酸氫鈉的質量,進而確定碳酸鈉的質量,再計算質量分數,為了防止空氣的二氧化碳被氫氧化鋇溶液吸收,在裝有氫氧化鋇溶液裝置的后面再連接裝有堿石灰的干燥管,據此答題.
解答 解:根據裝置圖可知,為測定樣品中Na2CO3的質量分數,先將樣品在試管中加熱,將生成氣體通往氫氧化鋇溶液中,根據氫氧化鋇溶液質量的質量的增加可知二氧化碳的質量,根據二氧化碳的質量可知樣品中碳酸氫鈉的質量,進而確定碳酸鈉的質量,再計算質量分數,為了防止空氣的二氧化碳被氫氧化鋇溶液吸收,在裝有氫氧化鋇溶液裝置的后面再連接裝有堿石灰的干燥管,
(1)根據上面的分析可知,該實驗所需要的裝置是②⑤⑥,所選用裝置的連接順序是B接H,G接I,
故答案為:②⑤⑥;B接H,G接I;
(2)為防止倒吸,停止加熱時,應先將B接口和H接口分開,
故答案為:應先將B接口和H接口分開;
(3)實驗裝置中盛堿石灰的U型管的作用是防止空氣的二氧化碳被氫氧化鋇溶液吸收而影響實驗的準確性,
故答案為:防止空氣的二氧化碳被氫氧化鋇溶液吸收而影響實驗的準確性;
(4)根據碳酸氫鈉分解的方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑可知,生成a g CO2時,則分解掉的碳酸氫鈉的質量為$\frac{84×2}{44}×ag$=$\frac{42}{11}a$g,所以W g樣品中所含Na2CO3的質量分數為$\frac{Wg-\frac{42}{11}ag}{Wg}$=$\frac{11W-42a}{11W}$,
故答案為:$\frac{11W-42a}{11W}$.
點評 本題考查較為綜合,以鈉的化合物為載體,綜合考查學生實驗能力和分析能力,注意把握物質的性質以及實驗原理,為解答該題的關鍵,題目難度中等.


科目:高中化學 來源:2016-2017學年江蘇省高二上10月階段測化學卷(解析版) 題型:推斷題
在下圖所示的物質轉化關系中,A是用于制造汽車發動機的耐高溫陶瓷材料,A由兩種元素組成,且兩種元素化合價的絕對值相等。常溫下,C、F、K是無色無味的氣體單質,D、H是固體單質。E是常見的兩性氧化物。B、G是汽車尾氣中的主要污染氣體,所 含元素均為第二周期元素
含元素均為第二周期元素 。反應②常用于汽車尾氣的處理。
。反應②常用于汽車尾氣的處理。
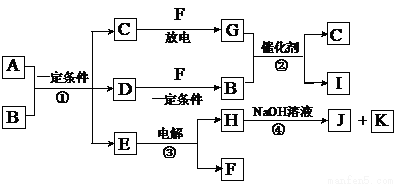
(1)C的電子式 。
(2)A的化學式 。
(3)反應③的化學方程式 。
(4)反應④的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 曲線a和b表示兩個反應過程的反應熱不同 | |
| B. | 曲線a一定表示反應是在無催化劑時的反應過程 | |
| C. | 增大壓強,X的轉化率一定增大 | |
| D. | 反應達平衡,升高溫度,平衡常數K值一定減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,1mol銅片投入含有4mol HNO3的濃硝酸中,銅片可以完全溶解 | |
| B. | Al與S直接化合可以得到Al2S3,Fe與S直接化合也可以得到Fe2S3 | |
| C. | 電解AlCl3、FeCl3、CuCl2的混合溶液中,陰極上依次析出Cu、Fe、Al | |
| D. | 等質量的鈉鋁合金中鋁的含量越大,與足量鹽酸反應時放出的氫氣越少 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 25℃時,0.1mol•L-1的三種溶液的pH關系為:pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa) | |
| B. | 25℃時,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液,c(H+)相等 | |
| C. | 25℃時,BaCO3在純水中的KSP比在Na2CO3溶液中的KSP大 | |
| D. | NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素 | Mn | Fe | |
| 電離能 | I1 | 717 | 759 |
| (kJ•mol-1) | I2 | 1 509 | 1 561 |
| I3 | 3 248 | 2 957 | |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 合成氨生產過程中將NH3液化分離,減小氨氣的濃度會導致化學平衡向左移動 | |
| B. | 合成氨工業中,使用鐵催化劑可加快正反應速率,提高N2、H2的轉化率 | |
| C. | 電解飽和食鹽水制燒堿采用離子交換膜法,可防止陰極室產生的C12進入陽極室 | |
| D. | 電解精煉銅時,同一時間內陽極溶解銅的質量比陰極析出銅的質量小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
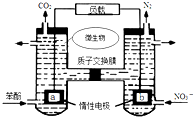
| A. | a電極發生還原反應 | |
| B. | H+由右室通過質子交換膜進入左室 | |
| C. | b電極反應式為:2NO3-+10e-+12H+═N2↑+6H2O | |
| D. | 電池工作時,電流由a電極沿導線流向b電極 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com