

分析 (1)根據圖示可知,儀器a為分液漏斗;
(2)二氧化硫、儀器不溶于濃硫酸,也不與濃硫酸反應,在裝置A中會產生氣泡,根據產生氣泡速度可以控制O2和SO2的流速;
(3)①二氧化硫為酸性氧化物,能夠使紫色石蕊試液變紅;裝置C中的氫硫酸與二氧化硫反應生成硫單質,體現了二氧化硫的氧化性;
②二氧化硫的漂白性是暫時的,加熱后會恢復原色,而氯水的漂白是永久的,據此設計檢驗方案;
(4)①二氧化硫和三氧化硫是大氣的污染物,需要用氧氣將裝置中二氧化硫和三氧化硫排出,從而被完全吸收;
②裝置G的作用是吸收二氧化硫,聯系二氧化硫的化學性質對各選項進行判斷;
③三氧化硫的熔沸點降低,所以二氧化硫和三氧化硫的混合氣體通過裝置F后,三氧化硫變成固體,即裝置F增加的mg為反應后生成的三氧化硫的質量,根據n=$\frac{m}{M}$計算出三氧化硫的物質的量,從而得出被氧化的二氧化硫的物質的量;
裝置G中二氧化硫與硝酸鋇反應生成硫酸鋇沉淀,產生的ng白色沉淀為硫酸鋇,根據n=$\frac{m}{M}$計算出生成硫酸鋇的物質的量,根據S原子守恒可知反應后剩余二氧化硫的物質的量,然后計算出二氧化硫的轉化率.
解答 解:(1)裝置圖中,充分濃硫酸的儀器a的名稱為分液漏斗,故答案為:分液漏斗;
(2)裝置A中盛放的是濃硫酸,可以將氣體充分混合、并干燥氣體,另外還可以根據產生氣泡速度控制通入的氧氣和二氧化硫的流速,通過觀察氣泡以便控制O2和SO2的流速,
故答案為:通過觀察氣泡以便控制O2和SO2的流速;
(3)①裝置B中盛放的是石蕊試液,二氧化硫溶于水生成弱酸亞硫酸,導致石蕊試液由紫色變為紅色;裝置C中盛放的是飽和硫化氫氣體,硫化氫能夠與二氧化硫反應生成S單質,該反應中二氧化硫化合價降低被還原,表現了氧化性,
故答案為:溶液由紫色變為紅色;氧化;
②經驗證D瓶中的溶液能使品紅試液褪色,二氧化硫的漂白性是暫時的、不穩定的,加熱后會褪色,而氯氣的漂白利用的是次氯酸的強氧化性,氯水的漂白是永久的,所以檢驗D瓶中含有SO2還是含有氯水的方法為:取褪色后的溶液加熱,若溶液變紅,則溶液中含有二氧化硫,否則含有氯水,
故答案為:取褪色后的溶液加熱,若溶液變紅,則溶液中含有二氧化硫,否則含有氯水;
(4)①使殘留在裝置中的SO2和SO3被充分吸收,故答案為:使殘留在裝置中的SO2和SO3被充分吸收;
②裝置G的作用是吸收并測定SO2,避免造成空氣污染,但是反應中會生成有毒的NO,
a.足量BaC12溶液:氯化鋇溶液不與二氧化硫反應,不能用氯化鋇溶液代替硝酸鋇,故a錯誤;
b.足量Ba(OH)2溶液能夠與二氧化硫反應,可以用氫氧化鋇溶液吸收二氧化硫,反應中沒有有毒氣體生成,故b正確;
c.鐵離子能夠將二氧化硫氧化成硫酸,硫酸與氯化鋇反應生成硫酸鋇沉淀,所以可用足量FeC13和BaC12的混合液代替硝酸鋇溶液,反應中不會生成有毒氣體,故c正確;
d.足量NaHSO3溶液:亞硫酸氫鈉溶液不與二氧化硫反應,無法代替裝置G,故d錯誤;
故答案為:bc;
③由于三氧化硫的熔沸點降低,所以二氧化硫和三氧化硫的混合氣體通過裝置F后,三氧化硫變成固體,即裝置F增加的mg為反應后生成的三氧化硫的質量,則反應生成的三氧化硫的物質的量為:$\frac{mg}{80g/mol}$=$\frac{m}{80}$mol,所以反應中被氧化的二氧化硫為$\frac{m}{80}$mol,
裝置G中二氧化硫與硝酸鋇反應生成硫酸鋇沉淀,產生的ng白色沉淀為硫酸鋇,生成硫酸鋇的物質的量為:$\frac{ng}{233g/mol}$=$\frac{n}{233}$mol,根據S原子守恒,反應后剩余二氧化硫的物質的量為$\frac{n}{233}$mol,所以二氧化硫的轉化率為:$\frac{\frac{m}{80}mol}{\frac{m}{80}mol+\frac{n}{233}mol}$×100%=$\frac{\frac{m}{80}}{\frac{m}{80}+\frac{n}{233}}×100%$,
故答案為:$\frac{\frac{m}{80}}{\frac{m}{80}+\frac{n}{233}}×100%$.
點評 本題考查了性質實驗方案的設計,題目難度中等,明確二氧化硫的性質及實驗目的為解答關鍵,注意掌握性質實驗方案設計與評價的原則,(4)②為難點、易錯點,需要明確裝置中質量變化的含義,試題培養了學生的分析能力及化學實驗能力.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ①②④ | C. | ①②③④ | D. | ①③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
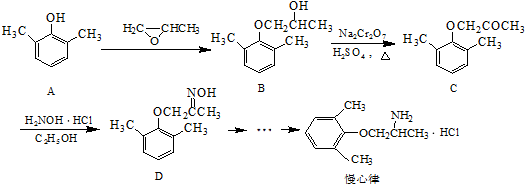
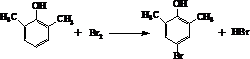 .
. .
.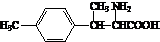 .
.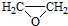 ).寫出以鄰甲基苯
).寫出以鄰甲基苯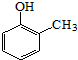 )和乙醇為原料制備
)和乙醇為原料制備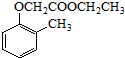 的合成路線流程圖(無機試
的合成路線流程圖(無機試查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 有機物A不能使溴的四氯化碳溶液褪色 | |
| B. | 胡妥油可以發生加成反應和氧化反應 | |
| C. | 有機物A與胡妥油互為同系物 | |
| D. | 1 mol胡妥油完全燃燒消耗313.6 L的氧氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 金屬離子 | 開始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.5 | 8.0 |
| Cu2+ | 5.2 | 6.7 |
| Fe2+ | 5.8 | 8.8 |
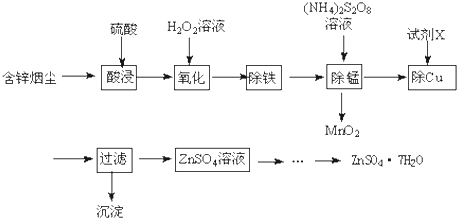
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
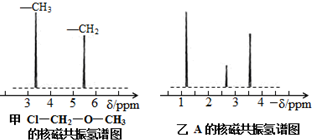
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁片和稀鹽酸反應 | B. | 氫氧化鋇晶體和氯化銨反應 | ||
| C. | 灼熱的碳與CO2反應 | D. | 甲烷在氧氣中燃燒 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 實 驗 | 現 象 | 結論 | |
| A | 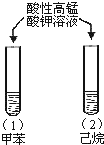 | 試管(1)中紫色褪去, 試管(2)中紫色未褪 | 苯環使甲基的活性增強 |
| B | 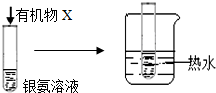 | 試管內壁有 銀鏡生成 | 有機物X中一定含有醛基 |
| C | 向淀粉溶液中加入稀硫酸,水浴加熱,一段時間后,再加入新制的氫氧化銅懸濁液并加熱 | 未見磚紅色沉淀 | 淀粉未水解 |
| D | 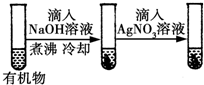 | 最后一只試管中有淺黃色沉淀 | 有機物中含有溴原子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com