

分析 (1)若甲、乙、丙、丁均為化合物,且焰色反應均呈黃色,即都含有鈉元素,丙是淡黃色固體,所以丙為過氧化鈉,常溫下X是一種無色無味氣體且能與過氧化鈉反應,所以X為二氧化碳,根據題中的各物質轉化關系可推知,丁為碳酸鈉,可以推知乙為氫氧化鈉,甲為氧化鈉,據此答題;
(2)若甲、乙、丙、丁都含有地殼中含量最多的金屬元素,即含有鋁元素,X、丁溶液的焰色反應均為紫色(透過藍色鈷玻璃),說明X、丁含有鉀元素,丙受熱時分解生成乙,則丙為氫氧化鋁,乙為氧化鋁,根據題中的各物質轉化關系可推知,甲為鋁,丁為偏鋁酸鉀,X為氫氧化鉀,據此答題.
解答 解:(1)若甲、乙、丙、丁均為化合物,且焰色反應均呈黃色,即都含有鈉元素,丙是淡黃色固體,所以丙為過氧化鈉,常溫下X是一種無色無味氣體且能與過氧化鈉反應,所以X為二氧化碳,根據題中的各物質轉化關系可推知,丁為碳酸鈉,可以推知乙為氫氧化鈉,甲為氧化鈉,
①氧化鈉和二氧化碳反應生成碳酸鈉的化學方程式為Na2O+CO2═Na2CO3,
故答案為:Na2O+CO2═Na2CO3;
②過氧化鈉與二氧化碳的反應中過氧化鈉既是氧化劑又是還原劑,每摩爾過氧化鈉在反應過程中轉移1mol電子,生成1mol碳酸鈉,所以有0.2mol碳酸鈉生成時,電子轉移的數目為0.2NA,
故答案為:Na2O2;0.2NA;
(2)若甲、乙、丙、丁都含有地殼中含量最多的金屬元素,即含有鋁元素,X、丁溶液的焰色反應均為紫色(透過藍色鈷玻璃),說明X、丁含有鉀元素,丙受熱時分解生成乙,則丙為氫氧化鋁,乙為氧化鋁,根據題中的各物質轉化關系可推知,甲為鋁,丁為偏鋁酸鉀,X為氫氧化鉀,
①如圖中五個轉化中屬于氧化還原反應有甲→乙是鋁生成氧化鋁,甲→丁是鋁與氫氧化鉀反應生成偏鋁酸鉀,其余均為非氧化還原反應,
故選A;
②鋁和氫氧化鉀生成偏鋁酸鉀的離子方程式為2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案為:2Al+2OH-+2H2O═2AlO2-+3H2↑;
③溶液中生成的氫氧化鋁能夠凈水,其原因是Al(OH)3能吸附水中的懸浮物,
故答案為:Al(OH)3能吸附水中的懸浮物.
點評 本題是考查無機物推斷、常用化學用語,難度中等,掌握元素化合物的性質是解題的關鍵,需要學生熟練掌握元素化合物知識,注意特殊的顏色與特殊反應是推斷的突破口.


科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ②④ | C. | ④⑥ | D. | ②⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某化學學習小組欲探究己烷的性質,用己烷進行下利實驗:
某化學學習小組欲探究己烷的性質,用己烷進行下利實驗:
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| Ⅰ實驗結果 | Ⅱ回答問題 |
| ①取原溶液少許,滴加足量氯水,產生沉淀;過濾,濾液加CCl4,振蕩后,CCl4層未變色. | ①該步實驗說明溶液中不存在Br-離子I-. |
| ②取原溶液少許,加入銅片和稀硫酸共熱,產生無色氣體,該氣體遇空氣立即變為紅棕色. | ②該步實驗發生反應的離子方程式為 8H++2NO3-(稀)+3Cu=3Cu2++2NO↑+4H2O. |
| ③取原溶液少許,加鹽酸酸化后,加入氨水有白色沉淀生成,繼續加入過量氨水,沉淀不消失. | ③產生白色沉淀的離子方程式為Al3++3NH3•H2O=Al(OH)3↓+3NH4+. |
| ④取原溶液少許,滴加2滴酸性高錳酸鉀溶液,紫色立即褪去. | ④該步實驗說明溶液中存在SO32-離子. |
| ⑤取原溶液少許,加足量Ba(NO3)2溶液產生白色沉淀,過濾;往洗滌后的沉淀中加入足量鹽酸,沉淀部分溶解,有無色氣體產生. | ⑤未溶解的白色沉淀是BaSO4;將氣體通入品紅溶液的現象是品紅溶液褪色. |
| ⑥取步驟⑤所得濾液,加HNO3酸化后,再加AgNO3溶液,溶液中析出白色沉淀. | ⑥該步驟是否有意義有(填“有”或“無”). |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 2H2O+O2↑,鐵離子會加速H2O2分解,使洗滌劑失去殺菌作用;2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑,Fe3+與CO32-水解相互促進,使洗滌劑失去去污能力.
2H2O+O2↑,鐵離子會加速H2O2分解,使洗滌劑失去殺菌作用;2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑,Fe3+與CO32-水解相互促進,使洗滌劑失去去污能力.查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用含1mol FeCl3的溶液制備成Fe(OH)3膠體,其中膠粒數為NA | |
| B. | 12g金剛石中含有的共價鍵數為4 NA | |
| C. | 常溫常壓下,14 g CO和N2的混合氣體中,含有原子數為NA | |
| D. | 1 L 1 mol/L NH4Cl溶液中含有NH4+數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
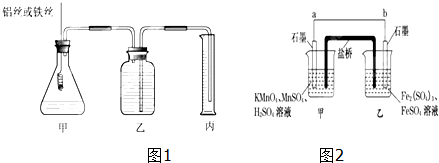
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4LH2O含有的分子數為NA | |
| B. | 2.7g金屬鋁無論與強堿還是強酸作用時失去電子數目均為0.3NA | |
| C. | 22.4LN2分子中所含原子數為2 NA | |
| D. | 10.6g Na2CO3(Na2CO3 化學式量為106)固體含有的Na+離子數為0.1NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com