
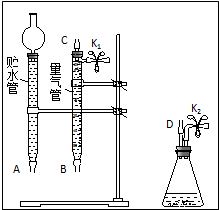
 某課外活動小組對“外界條件對銅與稀硝酸反應速率的影響”作了如下探究.
某課外活動小組對“外界條件對銅與稀硝酸反應速率的影響”作了如下探究.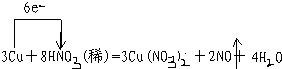 .
.| 實驗 編號 | 稀硝酸的濃度/(mol/L) | 稀硝酸的體積/mL | 溫度 /℃ | 時間 /min | 收集氣體 的體積/mL |
| ① | a | V | 25 | t1 | V1 |
| ② | V | ||||
| ③ | V |
分析 (1)①根據銅與稀硝酸反應中,銅做還原劑被氧化,而稀硝酸中的氮元素被還原為NO,根據得失電子數守恒來計算;
②從所給的藥品和儀器可知,本題可以探究硝酸濃度的不同或溫度的不同對反應速率的影響;
③根據題意可知,此裝置應為排水量氣裝置,而D為反應的發生裝置,連接量氣管將量氣管中的水排出,即量氣管起排水量氣的作用,而貯水管起到貯水的作用,故橡膠軟管的應D接C接B接A,據此分析;
④由于量氣管起到收集NO的作用,故將錐形瓶到量氣管間的空氣排干凈即可,據此分析;
(2)要設計實驗探究濃度對化學反應速率的影響,則必須保持其他影響反應速率的影響因素一致,據此分析.
解答 解:(1)①因銅失去電子,HNO3得到電子,銅做還原劑被氧化,而稀硝酸中的氮元素被還原為NO,故化學方程式為: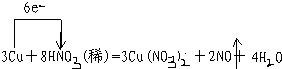 ,故答案為:
,故答案為: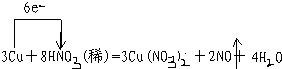 ;
;
②從所給的藥品和儀器可知,本題可以探究硝酸濃度的不同或溫度的不同對反應速率的影響,而要探究一個影響因素,則必須保持其他影響因素一致,故若探究硝酸濃度對反應速率的影響,則溫度相同,反之,若溫度不同,則硝酸濃度相同;測定反應速率的快慢,可以通過測定相同時間內產生氣體體積或
產生相同體積的氣體所需的時間來進行,
故答案為:相同稀硝酸濃度、不同溫度(或相同溫度、不同稀硝酸濃度);相同時間內產生氣體體積(或產生相同體積的氣體所需的時間);
③根據題意可知,此裝置應為排水量氣裝置,而D為反應的發生裝置,生成的氣體通過軟管進入量氣管,將其中的水排出,即量氣管起排水量氣的作用,排出的水進入貯水管,而貯水管起到貯水的作用,故橡膠軟管的應D接C接B接A,故圖為: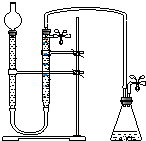 ,故答案為:
,故答案為: ;
;
④由于量氣管起到收集NO的作用,故要將錐形瓶到量氣管間的空氣排干凈,從從K2處的橡膠管向裝置中通入CO2,松開K1彈簧夾,在K1處接盛有澄清石灰水的燒杯,直到石灰水變渾濁時為止,故答案為:松開K1彈簧夾,接導管通入澄清石灰水至出現白色渾濁為止;
(2)要設計實驗探究濃度對化學反應速率的影響,則必須保持其他影響反應速率的影響因素一致,故若②的稀硝酸的濃度為b,則應保持溫度與①的相同即25℃,而由于稀硝酸的濃度不同,故反應速率不同,則在相同的時間段內,收集到的其他的體積要不同,即時間為t1,則收集到的氣體體積應為V2;或收集相同體積的氣體時,所需的時間不同,即收集到的氣體體積也為V1,但所需時間為t2;
既然①②對比試驗探究的是濃度的不同對反應速率的影響,則①③探究的是溫度的不同對反應速率的影響,故③中溫度應為50℃,則稀硝酸的濃度應為a,而由于溫度不同,故反應速率不同,則在相同的時間段內,收集到的其他的體積要不同,即時間為t1,則收集到的氣體體積應為V2;或收集相同體積的氣體時,所需的時間不同,即收集到的氣體體積也為V1,但所需時間為t2.故答案為:
| 實驗 編號 | 稀硝酸的濃度/(mol/L) | 稀硝酸的體積/mL | 溫度 /℃ | 時間 /min | 收集氣體 的體積/mL |
| ① | a | V | 25 | t1 | V1 |
| ② | b | V | 25 | t1(或t2) | V2(或V1) |
| ③ | a(或b) | V | 50 | t2(或t1) | V1(或V2) |
點評 本題考查了影響反應速率的因素,應注意的是要探究某個因素對反應速率的影響,則必須保持其他影響因素一致,且可以通過測量在相同時間段內收集到的氣體體積的大小或收集相同體積的氣體所需的時間來判斷反應速率的快慢.


科目:高中化學 來源: 題型:解答題
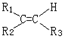 $\stackrel{氧化}{→}$
$\stackrel{氧化}{→}$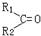 +R3COOH
+R3COOH查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氨水和氫氧化鈉 | B. | 硫酸銨和氯化鋇 | C. | 硝酸亞鐵和鹽酸 | D. | 電石和鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
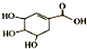
| A. | 分子式為C7H6O5 | B. | 可發生取代反應 | ||
| C. | 可使酸性高錳酸鉀溶液褪色 | D. | 不能與溴水發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
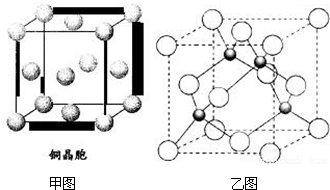
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
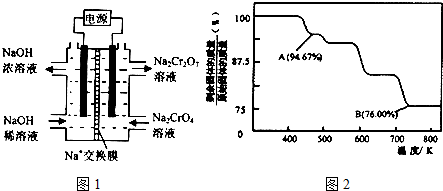
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 →CH3-CHO+H2O
→CH3-CHO+H2O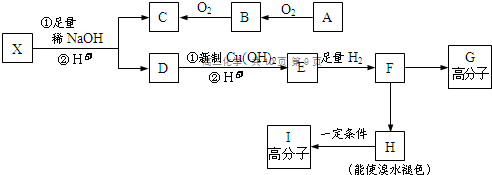
 ;F→H的反應類型是消去反應.
;F→H的反應類型是消去反應. .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1種 | B. | 2種 | C. | 3種 | D. | 4種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 現有A、B、C、D、E、F原子序數依次增大的六種元素,它們位于元素周期表的前四周期,B元素含有3個能級,且每個能級所含的電子數相同;D的原子核外有8個運動狀態不同的電子;E元素與F元素處于同一周期相鄰的族,它們的原序數相差3,且E元素的基態原子有4個未成對電子,請回答下列問題:
現有A、B、C、D、E、F原子序數依次增大的六種元素,它們位于元素周期表的前四周期,B元素含有3個能級,且每個能級所含的電子數相同;D的原子核外有8個運動狀態不同的電子;E元素與F元素處于同一周期相鄰的族,它們的原序數相差3,且E元素的基態原子有4個未成對電子,請回答下列問題: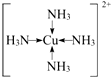 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com