
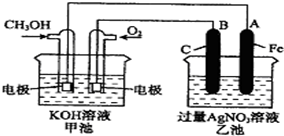
 如圖是一個化學過程的示意圖,已知甲池的總反應式為:2CH3OH+3O2+4KOH═2K2CO3+6H2O則下列說法中不正確的是( )
如圖是一個化學過程的示意圖,已知甲池的總反應式為:2CH3OH+3O2+4KOH═2K2CO3+6H2O則下列說法中不正確的是( )| A. | 甲池是燃料電池,其中通入氧氣的一極是原電池的正極 | |
| B. | 乙池是電解池,鐵電極是陰極,一段時間后會析出金屬銀 | |
| C. | 甲池是電解池,乙是原電池 | |
| D. | 甲池一段時間后溶液的pH值會變小 |
分析 根據反應方程式知,甲裝置是燃料電池,通入甲醇的一極為負極,通入氧氣的一極為正極;乙有外加電源,所以是電解池,石墨與原電池的正極相連,所以B石墨電極是陽極,Fe為陰極,陰極上銀離子得電子生成Ag,結合反應方程式判斷溶液的pH.
解答 解:A.甲裝置是燃料電池,通入甲醇的一極為負極,通入氧氣的一極為正極,故A正確;
B.Fe與原電池的負極相連,Fe為陰極,陰極上銀離子得電子生成Ag,故B正確;
C.甲裝置是燃料電池,乙有外加電源,是電解池,故C錯誤;
D.甲池的總反應式為:2CH3OH+3O2+4KOH═2K2CO3+6H2O,反應消耗KOH,溶液的堿性減小,則pH減小,故D正確.
故選C.
點評 本題考查了原電池原理和電解池原理的應用,明確電極判斷方法、電極反應的書寫等是解題關鍵,側重于考查學生的分析能力,題目難度不大.


 口算題天天練系列答案
口算題天天練系列答案科目:高中化學 來源: 題型:解答題
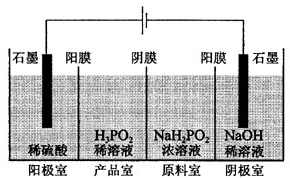 次磷酸(H3PO2)是一種精細磷化工產品,具有較強還原性.回答下列問題:
次磷酸(H3PO2)是一種精細磷化工產品,具有較強還原性.回答下列問題:查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上第一次月考化學卷(解析版) 題型:填空題
如圖所示,當關閉K時,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始時體積V(A)=V(B)=a L,在相同溫度和有催化劑存在的條件下,兩容器各自發生下列反應:2X(g)+2Y(g)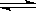 Z(g)+2W(g)△H<0達到平衡(Ⅰ)時V(B)=0.9a L,試回答:
Z(g)+2W(g)△H<0達到平衡(Ⅰ)時V(B)=0.9a L,試回答:
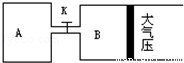
(1)B中X的轉化率α(X)B為_________。
(2)A中W和B中Z的物質的量的比較:n(W)A __________________ n(Z)B(填<、>、或=)
(3)打開K,過一段時間重新達平衡(Ⅱ)時,B的體積為_________升(用含a的代數式表示,連通管中氣體體積不計)
(4)要使B容 器恢復原來反應前的體積,可采取的措施是____________________。
器恢復原來反應前的體積,可采取的措施是____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| A | |||||||
| B | C | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
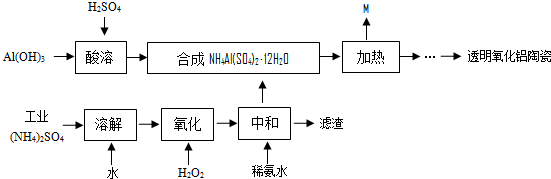
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D | |
| 強電解質 | NaCl | H2SO4 | HClO | HNO3 |
| 弱電解質 | HF | BaSO4 | CaCO3 | CH3COOH |
| 非電解質 | Cl2 | CS2 | C2H5OH | SO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
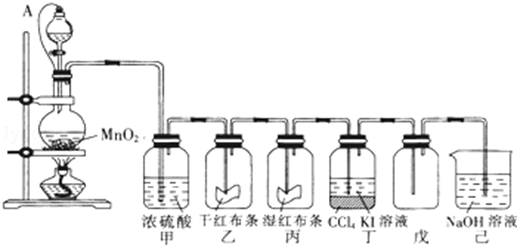
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 熔點:Na-K合金<Na<氯化鈉 | |
| B. | 非金屬氫化物的穩定性順序:H2O>H2S>H2Se,HCl<H2S<PH3 | |
| C. | CO2與Na2O2反應只生成Na2CO3和O2,故SO2與Na2O2反應只生成Na2SO3和O2 | |
| D. | 同一原子中,2p、3p、4p能級的軌道數依次增多 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com