
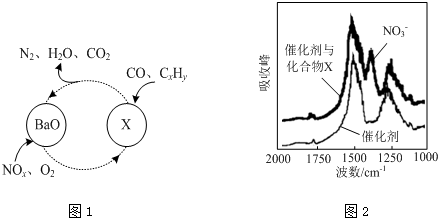
分析 (1)根據化合價降低為氧化劑被還原判斷;根據傅里葉紅外光譜圖(如圖2所示)確定化合物X含硝酸根;
(2)根據NOx與NH3的直接反應,實現無害轉化,則生成氮氣和水,據此書寫方程式;
(3)根據反應的離子方程式進行計算.
解答 解:(1)在圖1所示的轉化中N、O化合價降低為氧化劑被還原;由傅里葉紅外光譜圖(如圖2所示)確定化合物X含硝酸根,再結合圖一由鋇離子參與,所以X為Ba(NO3)2;
故答案為:N、O;Ba(NO3)2;
(2)因為NOx與NH3的直接反應,實現無害轉化,則生成氮氣和水,所以當NO與NO2的物質的量之比為4:1時,發生反應的化學方程式為8NH3+8NO+2NO2=9N2+12H2O,
故答案為:8NH3+8NO+2NO2=9N2+12H2O;
(3)由2NH4++3ClO-=N2↑+3Cl-+2H++3H2O得,處理廢水產生了0.448L即$\frac{0.448L}{22.4L/mol}$=0.02mol N2(標準狀況),則需消耗濃度為0.5mol•L-1的次氯酸鈉的體積為$\frac{0.02×3}{0.5}$×1000ml=120ml,
故答案為:120.
點評 本題重點考查了氧化還原反應,注意把握氧化還原反應的本質是解決本題的關鍵,難度中等,注意化合價降低為氧化劑被還原,化合價升高為還原劑被氧化.


科目:高中化學 來源: 題型:選擇題
| A. | X與Y形成的兩種化合物中陰、陽離子的個數比均為1:2,且均能與水反應 | |
| B. | 根據非金屬性強弱,不可能由Z的最高價氧化物制出W的最高價氧化物 | |
| C. | Y的簡單氫化物的沸點和熱穩定性均大于R的簡單氫化物 | |
| D. | 向兩份BaCl2溶液中分別通入RY2、WY2,均無白色沉淀生成,但一段時間后,通入RY2的一份中可能產生沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol丙烯酸中含有雙鍵的數目為0.1NA | |
| B. | 2.0g重水(2H2O)中含有的質子數為1.0 NA | |
| C. | 標準狀況下,11.2 LCl2通入足量的石灰乳中制備漂白粉,轉移的電子數為NA | |
| D. | 標準狀況下,2.24LSO3中含有的O原子的數目為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
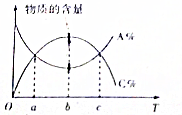 對于反應mA+nB?pC,在其它條件不變時,A與C兩物質的物質的量隨溫度的變化情況如圖所示,則下列說法正確的是( )
對于反應mA+nB?pC,在其它條件不變時,A與C兩物質的物質的量隨溫度的變化情況如圖所示,則下列說法正確的是( )| A. | 該反應為吸熱反應 | |
| B. | 在a,c時刻,正逆反應速率相等 | |
| C. | 若橫軸為壓強,則存在m+n<p | |
| D. | b時刻正逆反應速率大于c時刻的正逆反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
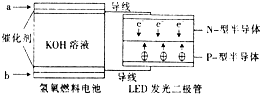 LED系列產品是被看好的一類節能新產品.如圖是一種氫氧燃料電池驅動LED 發光的裝置.下列有關敘述正確的是( )
LED系列產品是被看好的一類節能新產品.如圖是一種氫氧燃料電池驅動LED 發光的裝置.下列有關敘述正確的是( )| A. | a處通入氫氣,發生還原反應 | |
| B. | b處為電池正極,發生了還原反應 | |
| C. | 該裝置中只涉及兩種形式的能量轉化 | |
| D. | P-型半導體連接的是電池負極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗目的 | 主要儀器 | 試劑 |
| A | 配制480mL 2mol/L的NaOH溶液 | 膠頭滴管、燒杯、玻璃棒、托盤天平、480mL容量瓶 | NaOH固體、蒸餾水 |
| B | 測定中和熱 | 燒杯、玻璃棒、紙板、保溫塑料、溫度計 | 50mL0.5mol/LNaOH溶液與50mL0.5mol/L鹽酸 |
| C | 測定生成H2速率 | 分液漏斗、錐形瓶、針筒、鐵架臺 | Zn粒、稀硫酸 |
| D | 濃硫酸脫水性 | 分液漏斗、試管 | 蔗糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

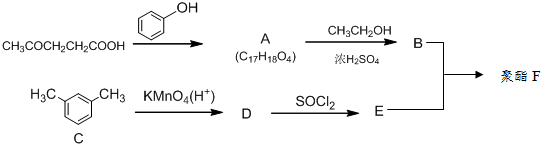
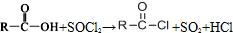 ②
② (R、R′表示烴基)
(R、R′表示烴基)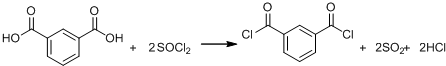
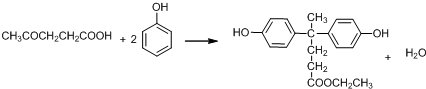
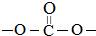 結構.
結構.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
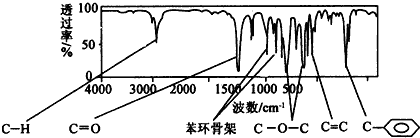
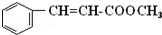 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com