
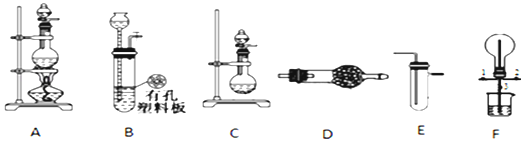
分析 (1)利用濃氨水滴入生石灰產生氨氣,與制取干燥氨氣可以用堿石灰干燥氨氣;
(2)依據制備氯氣裝置是利用二氧化錳和濃鹽酸加熱反應,生成的氯氣中含有氯化氫和水蒸氣,通過飽和食鹽水除去氯化氫,通過濃硫酸除去水蒸氣;
(3)實驗時打開開關1、3,關閉2向燒瓶中通入氯氣,然后關閉1、3,打開2,向燒瓶中緩慢通入一定量的氨氣,實驗一段時間后燒瓶內出現濃厚的白煙并在容器內壁凝結,依據反應化學方程式判斷是生成的氯化氫和氨氣反應生成的氯化銨;依據銨根離子的檢驗方法是和堿反應生成氨氣設計實驗檢驗;
(4)氯氣的氧化性強于碘,能夠置換碘,碘的四氯化碳為紫紅色;
(5)二氧化硫具有弱的氧化性能夠氧化硫化氫生成留單質;二氧化硫、硫化氫都有毒,應進行尾氣處理.
解答 解:(1)為制取干燥氨氣,可將裝置C連接D點的干燥的氨氣,裝置C中的燒瓶內固體宜選用堿石灰或者生石灰;
故答案為:bd;
(2)依據制備氯氣裝置是利用二氧化錳和濃鹽酸加熱反應,生成的氯氣中含有氯化氫和水蒸氣,通過飽和食鹽水除去氯化氫,通過濃硫酸除去水蒸氣;
故答案為:飽和食鹽水;
(3)實驗時打開開關1、3,關閉2向燒瓶中通入氯氣,然后關閉1、3,打開2,向燒瓶中緩慢通入一定量的氨氣,實驗一段時間后燒瓶內出現濃厚的白煙并在容器內壁凝結,已知氯氣與氨氣可發生反應:3Cl2+2NH3→N2+6HCl,依據反應化學方程式判斷是生成的氯化氫和過量氨氣反應生成的氯化銨;銨根離子的檢驗方法是,取少量固體于試管中,加入適量NaOH溶液并加熱,在管口用濕潤的紅色石蕊試紙檢驗產生的氣體,若濕潤的紅色石蕊試紙變藍,證明固體中有NH4+;
故答案為:氯氣;取少量固體于試管中,加入適量NaOH溶液并加熱,在管口用濕潤的紅色石蕊試紙檢驗產生的氣體,若濕潤的紅色石蕊試紙變藍,證明固體中有NH4+;
(4)裝置A為制取氯氣的裝置,制取的氯氣通入到盛有碘離子的鹽溶液中,氯氣與碘離子發生氧化還原反應生成碘單質,E中得到碘單質的水溶液,向裝置E中加入CCl4溶液,將碘萃取到CCl4中,CCl4比水中,在下層,下層為紫紅色;
故答案為:E中下層為紫紅色;
(5)二氧化硫氧化硫化氫生成硫單質,2H2S+SO2=3S↓+2H2O;F燒杯是吸收剩余氣體二氧化硫或硫化氫有毒氣體的作用;
故答案為:2H2S+SO2=3S↓+2H2O;吸收尾氣.
點評 本題考查物質性質的實驗驗證和實驗設計方法,反應現象的分析判斷,裝置選擇,掌握實驗基礎和物質性質是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:解答題
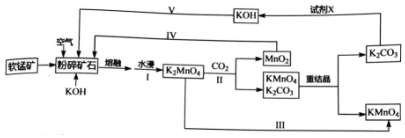
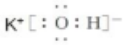 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
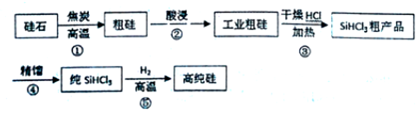
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 離子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定物質的量濃度的溶液配制過程中,仰視定容,所得溶液的濃度偏大 | |
| B. | 相同體積和相同物質的量濃度的不同溶液里所含溶質的物質的量相同 | |
| C. | 溶液中溶質質量分數為w,密度為ρ g/cm3,溶質摩爾質量為M g/mol的溶液的物質的量濃度為$\frac{pw}{M}$mol/L | |
| D. | 10 mol/L的濃鹽酸與H2O等質量混合所得混合液的濃度為5 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | m+n<p | B. | 平衡向逆反應方向移動 | ||
| C. | A的轉化率降低 | D. | C的體積分數增加 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 澄清石灰水跟過量CO2氣體反應:Ca(OH)2+CO2=CaCO3↓+H2O | |
| B. | 稀硫酸與Cu反應:2H++Cu=Cu2++H2↑ | |
| C. | 腐蝕法制作印刷線路板:2Fe3++Cu=2Fe2++Cu2+ | |
| D. | 鐵粉加入AgNO3溶液中:Fe+Ag+=Fe2++Ag |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2O與D2O互為同位素 | B. | 氟離子的結構示意圖: | ||
| C. | 工業上用電解熔融氧化鎂制單質鎂 | D. | 工業上用電解飽和食鹽水制取氯氣 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com