
| A. | 25℃時,pH=13的1.0LBa(OH)2溶液中含有的OH-數目為0.2NA | |
| B. | 標準狀況下,2.24L乙烷中含有的極性鍵數目為0.6NA | |
| C. | 室溫下,3g甲醛和乙酸的混合物中含有的原子數目為0.8NA | |
| D. | 56g鐵與足量稀硫酸反應轉移的電子數為3NA |
分析 A.pH=13的氫氧化鋇溶液中氫氧根離子濃度為0.1mol/L,1L該溶液中含有0.1mol氫氧根離子;
B.乙烷分子中含有的極性鍵為碳氫鍵,乙烷分子中含有6個碳氫鍵;
C.甲醛和乙酸最簡式為CH2O,計算3.0gCH2O中含有的原子數即可;
D.鐵與稀硫酸反應生成的是亞鐵離子,56g鐵為1mol,完全反應轉移了2mol電子.
解答 解:A.pH=13的1.0LBa(OH)2溶液中含有氫氧根離子的物質的量為:0.1mol/L×1L=0.1mol,所以含有的OH-數目等于0.1NA,故A錯誤;
B.標況下2.24L乙烷的物質的量為0.1mol,0.1mol乙烷分子中含有0.6mol極性鍵碳氫鍵,含有的極性鍵數目為0.6NA,故B正確;
C.甲醛和乙酸最簡式為CH2O,3.0 g甲醛和乙酸的混合物中含有碳原子的個數,只需要計算3.0gCH2O中碳原子物質的量=$\frac{3.0g}{30g/mol}$=0.1mol,0.1molCH2O中含有0.4mol原子,含有的原子數為0.4NA,故C錯誤;
D.56g鐵的物質的量為為:$\frac{56g}{56g/mol}$=1mol,1mol鐵與稀硫酸完全反應生成1mol亞鐵離子,轉移了2mol電子,轉移的電子數為2NA,故D錯誤;
故選B.
點評 本題考查阿伏加德羅常數的有關計算和判斷,題目難度中等,注意掌握好以物質的量為中心的各化學量與阿伏加德羅常數的關系,準確弄清分子、原子、原子核內質子中子及核外電子的構成關系;D為易錯點,注意反應生成亞鐵離子.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 英國科學家近日研發出一種名為NOTT-202a的新型多孔材料,空氣中其他氣體可自由通過這些孔洞,但CO2會被殘留.該材料的分子結構單元是以銦原子為中心,周圍是以各種有機分子鏈條編織成的“籠子”,整體上看呈現出多孔特征,有些類似自然界中的蜂窩結構.下列有關說法正確的是( )
英國科學家近日研發出一種名為NOTT-202a的新型多孔材料,空氣中其他氣體可自由通過這些孔洞,但CO2會被殘留.該材料的分子結構單元是以銦原子為中心,周圍是以各種有機分子鏈條編織成的“籠子”,整體上看呈現出多孔特征,有些類似自然界中的蜂窩結構.下列有關說法正確的是( )| A. | 該材料是一種新型金屬有機材料 | |
| B. | 該材料能捕集CO2,是因為CO2與該材料發生了化學反應 | |
| C. | 該材料捕集11.2L CO2后,增重22g | |
| D. | 可利用該材料將空氣中的CO2完全捕集,從而控制溫室效應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 的電離程度分別用α1、α2表示,則α1小于α2(填“大于”、“小于”、“等于”或“無法確定”)
的電離程度分別用α1、α2表示,則α1小于α2(填“大于”、“小于”、“等于”或“無法確定”)查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 明礬溶液中滴加Ba(OH)2溶液至SO42-完全沉淀:Al3++Ba2++SO42-+3OH-═BaSO4↓+Al(OH)3↓ | |
| B. | Fe(OH)3溶于氫碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 銅溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2 NO↑+4H2O | |
| D. | MgSO4溶液與Ba(OH)2溶液混合:SO42-+Ba2+═BaSO4↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工藝師可利用氫氟酸刻蝕石英制作藝術品,說明氫氟酸的酸性很強 | |
| B. | 水晶項鏈和光導纖維的主要成分是相同的 | |
| C. | 粗硅的制備及提純單晶硅均涉及到氧化還原反應 | |
| D. | 我國自主研發的“龍芯1號”CPU芯片與神舟六號飛船使用的太陽能電池都用到硅 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
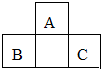 短周期元素A、B、C的位置如圖所示,已知B、C兩元素的原子序數之和是A元素的4倍,則A、B、C依次是( )
短周期元素A、B、C的位置如圖所示,已知B、C兩元素的原子序數之和是A元素的4倍,則A、B、C依次是( )| A. | Be、Na、Al | B. | C、Al、P | C. | B、Mg、Si | D. | O、P、Cl |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com