
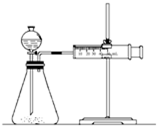
 影響化學反應速率的因素很多,某校化學小組用實驗的方法進行探究.
影響化學反應速率的因素很多,某校化學小組用實驗的方法進行探究.| 實驗步驟 | 現象 | 結論 |
| ①分別取等體積的2mol/L的硫酸于試管中 ② | 反應速率Mg>Fe, Cu不反應 | 金屬的性質越活潑, 反應速率越快 |
| △V |
| △t |
| △V |
| △t |


 尖子生新課堂課時作業系列答案
尖子生新課堂課時作業系列答案 英才計劃同步課時高效訓練系列答案
英才計劃同步課時高效訓練系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、c(HA)>c(HB) |
| B、c(A-)>c(B-) |
| C、c(H+)>c(OH-) |
| D、c(A-)+c(B-)>c(Na+) |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
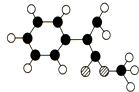
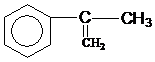 出發來合成A,其合成路線如下:
出發來合成A,其合成路線如下: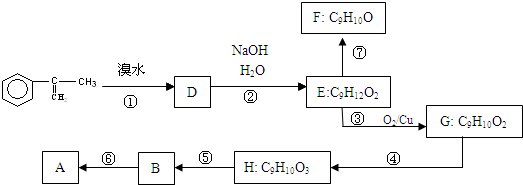
查看答案和解析>>
科目:高中化學 來源: 題型:
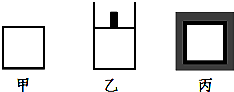 T℃時,容積固定為1L的密閉容器甲中充入2molSO2、1molO2,發生反應:2SO2(g)+O2(g)?2SO3(g)△H<0,維持溫度為T℃,4min后達到平衡,測得平衡時n(SO3)=1.2mol.
T℃時,容積固定為1L的密閉容器甲中充入2molSO2、1molO2,發生反應:2SO2(g)+O2(g)?2SO3(g)△H<0,維持溫度為T℃,4min后達到平衡,測得平衡時n(SO3)=1.2mol.查看答案和解析>>
科目:高中化學 來源: 題型:
| A、由水電離的c(H+):①=②=③=④ |
| B、等體積的①、②、④溶液分別與足量鋁粉反應,生成H2的量:②最大 |
| C、將②、③溶液混合后,若pH=7,則消耗溶液的體積:②>③ |
| D、四種溶液均稀釋100倍后,溶液的pH:③>④>②>① |
查看答案和解析>>
科目:高中化學 來源: 題型:
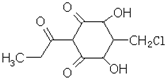
| A、該物質的分子式為:C10H7O5Cl |
| B、1mol該物質在常溫下最多可與3mol NaOH反應 |
| C、該物質遇FeCl3溶液不能發生顯色反應 |
| D、該物質可發生取代、氧化、消去反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com