
| A. | 0.5molO3與11.2LO2所含的分子數一定相等 | |
| B. | 25℃與60℃時,水的pH相等 | |
| C. | 中和等體積、等物質的量的濃度的鹽酸和醋酸所消耗的n(NaOH)相等 | |
| D. | 2SO2(g)+O2(g)=2SO3(g)和4SO2(g)+2O2(g)=4SO3(g)的△H相等 |
分析 A.沒有指出標準狀況下,無法計算氧氣的物質的量;
B.溫度不同,水電離出氫離子的濃度不同,則溶液的pH不相等;
C.鹽酸和醋酸都是一元酸,二者物質的量相等時消耗氫氧化鈉的物質的量相等;
D.焓變與化學計量數成正比,計量數不同則焓變不同.
解答 解:A.不是標準狀況下,無法計算11.2LO2的物質的量,故A錯誤;
B.25℃與60℃時水的電離程度不同,水的pH=-lgc(H+),則水的pH不相等,故B錯誤;
C.等體積、等物質的量的濃度的鹽酸和醋酸,兩溶液含有HCl和醋酸的物質的量相等,二者都是一元酸,則與氫氧化鈉溶液發生中和反應時消耗氫氧化鈉溶液的物質的量相等,故C正確;
D.反應2SO2(g)+O2(g)=2SO3(g)和4SO2(g)+2O2(g)=4SO3(g)的化學計量數不同,則兩個反應的△H一定不相等,故D錯誤;
故選C.
點評 本題考查了物質的量的計算,題目難度不大,涉及pH計算、反應熱與焓變、中和反應、物質的量的計算等知識,A為易錯點,注意明確標準狀況下氣體摩爾體積的使用條件,試題側重考查學生的分析能力及靈活應用能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | B的平均消耗速率為0.3mol/(L•min) | |
| B. | 升高溫度時,v正減小,v逆增大 | |
| C. | 若單位時間內生成的B和D的物質的量之比為3:1,則體系處于平衡狀態 | |
| D. | 平衡后,增大壓強,平衡將向正方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “接觸法”制H2SO4時,催化氧化階段的反應原理為:2SO2(g)+O2(g)$?_{△}^{催化劑}$2SO3(g)△H<0 | |
| B. | 海水提鎂的主要步驟為:海水$\stackrel{CaCO_{3}(s)}{→}$Mg(OH)2(s)$\stackrel{鹽酸}{→}$MgCl2(aq)$\stackrel{電解}{→}$Mg(l)+Cl2(g) | |
| C. | 普通水泥的主要成分是硅酸鈣 | |
| D. | 黏土的主要成分是三氧化二鋁. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用聚二氧化碳塑料會產生白色污染 | |
| B. | 聚二氧化碳塑料是通過聚合反應制得的 | |
| C. | 聚二氧化碳塑料與干冰互為同分異構體 | |
| D. | 聚二氧化碳塑干冰都屬于純凈物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗操作 | 實現現象 | 結論 | |
| A | 用飽和碳酸鈉溶液浸泡鍋爐沉積物后,過濾,洗滌,在所得沉淀物中再加入稀鹽酸 | 有氣泡產生 | 可除去鍋爐沉淀物中的CaSO4 |
| B | 某充滿NO2的密閉容器中,待反應平衡后,保持溫度不變,擴大容器體積 | 氣體顏色變淺 | 平衡2NO2(g)?N2O4(g)正向移動 |
| C | 向品紅溶液中通入某氣體 | 溶液褪色 | 該氣體是SO2 |
| D | 用潔凈鉑絲蘸取溶液置于酒精燈火焰上灼燒 | 火焰呈黃色 | 溶液中含Na+,無K+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl-的結構示意圖: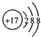 | |
| B. | 聚丙烯的結構簡式: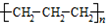 | |
| C. | 三氟化氮的電子式: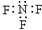 | |
| D. | 熔融硫酸氫鉀電離方程式:KHSO4$\frac{\underline{\;熔融\;}}{\;}$ K++H++SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用激光筆照射淀粉溶液和葡萄糖溶液,能產生光亮的“通路”的是淀粉溶液 | |
| B. | 將某氣體通入淀粉碘化鉀溶液中,溶液變藍色,該氣體一定是Cl2 | |
| C. | 向某溶液中加入AgNO3溶液,產生白色沉淀,該溶液中一定含Cl- | |
| D. | 向某稀溶液中加入少量NaOH溶液,未產生使濕潤的紅色石蕊試紙變藍的氣體,該溶液中一定 不含NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
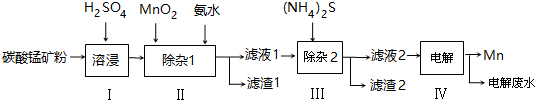
| 物質 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com