

分析 (1)s能級有一個軌道,最多排2個電子,p能級有3個軌道,每個軌道最多排2個電子,結合洪特規則分析;
(2)化學鍵的鍵能大于氫鍵的鍵能,氫鍵的鍵能大于分子間作用力;氫鍵對物質的物理性質產生影響,分子間氫鍵使物質的沸點升高,分子內氫鍵使物質的沸點降低;
(3)先確定VSEPR模型,然后在確定中心原子的雜化軌道類型;一般來說,相互之間排斥力的大小為:孤電子對間的排斥力>孤電子對與成鍵電子對間的排斥力>成鍵電子對間的排斥力;
(4)先計算一個氧化鈣分子的質量,再用均攤法求出一個晶胞含有的陰陽離子數,然后根據V=$\frac{m}{ρ}$求出其體積.
解答 解:(1)氧元素基態原子核外電子排布式為1s22s22p4,4個電子在三個軌道中排布,故未成對電子數為2個,故答案為:2;
(2)共價鍵的鍵能大于氫鍵的作用力,氫鍵的作用力還大于范德華力,故H2O分子內的O-H鍵、分子間的范德華力和氫鍵從強到弱依次為O-H鍵、氫鍵、分子間的范德華力;含分子間氫鍵的物質的沸點大于分子內氫鍵物質的沸點,因此原因是前者易形成分子間氫鍵,后者易形成分子內氫鍵.
故答案為:O-H鍵、氫鍵、范德華力;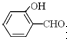 形成分子內氫鍵,而
形成分子內氫鍵,而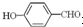 形成分子間氫鍵,分子間氫鍵使分子間作用力增大;
形成分子間氫鍵,分子間氫鍵使分子間作用力增大;
(3)H3O+價層電子對模型為四面體,氧原子采取sp3雜化.
H2O中O原子有兩對孤對電子,H3O+中O原子有一對孤對電子,因為孤電子對間的排斥力>孤電子對與成鍵電子對間的排斥力>成鍵電子對間的排斥力,導致H3O+中H-O-H鍵角比H2O中H-O-H鍵角大.
故答案為:sp3;H2O中O原子有兩對孤對電子,H3O+中O原子有一對孤對電子,排斥力較小;
(4)1個“CaO”的質量為$\frac{56g/mol}{N{\;}_{A}/mol}$=$\frac{56}{N{\;}_{A}}$,而用均攤法算出一個晶胞含有4個“CaO”,即一個晶胞質量為$\frac{56}{N{\;}_{A}}$×4=$\frac{224}{N{\;}_{A}}$g,又有ρ=$\frac{m}{ρ}$,則V=$\frac{m}{ρ}$,
V=$\frac{224}{N{\;}_{A}}$g÷ag/cm3=$\frac{224}{aN{\;}_{A}}$,則CaO晶胞體積為 $\frac{224}{aN{\;}_{A}}$.
故答案為:$\frac{224}{aN{\;}_{A}}$.
點評 本題把物質結構和性質與有機化合物的性質融合成一體,考查學生對元素推理、原子軌道雜化類型、分子空間結構、氫鍵、等電子體原理、晶胞結構等知識的掌握和應用能力.本題基礎性較強,難度較大,注意晶胞體積的計算方法.


科目:高中化學 來源: 題型:選擇題
| A. | 1L 1mol•L-1的兩種強酸溶液中,所含氫離子數目均為NA | |
| B. | T℃時,1 L pH=6純水中,含10-6NA個OH- | |
| C. | 1L濃度為1mol•L-1的Na2CO3溶液中含有NA個CO32- | |
| D. | 標準狀況下22.4LHCl氣體溶于水,其溶液中H+數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 足量的鈉在等物質的量的Cl2和O2中分別燃燒轉移電子數 | |
| B. | 等物質的量的KO2與CaO2分別與水反應生成 的氣體體積(相同條件下) | |
| C. | 100mL 1mol/L HNO3分別與1.4g Fe、2.8gFe完全反應時生成 的NO物質的量 | |
| D. | 等濃度等體積的鹽酸、NaOH溶液分別與一定量Al反應生成等質量氣體時轉移的電子數 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 二十二碳六烯酸,俗稱腦黃金,是一種對人體非常重要的不飽和脂肪酸,其結構簡式如圖.下列相關說法不正確的是( )
二十二碳六烯酸,俗稱腦黃金,是一種對人體非常重要的不飽和脂肪酸,其結構簡式如圖.下列相關說法不正確的是( )| A. | 該物質的分子式為:C22H32O2 | |
| B. | 該物質能使酸性高錳酸鉀溶液褪色 | |
| C. | 該物質一定條件下能發生取代反應 | |
| D. | 1mol該物質最多能與7molBr2發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | P和S屬于第三周期元素,P的第一電離能比S小 | |
| B. | Na和Rb屬于第ⅠA族元素,Rb失電子能力比Na強 | |
| C. | C和Si屬于第ⅣA族元素,Si比C更容易和氫氣反應 | |
| D. | Cl和Br屬于第ⅦA族元素,HClO4酸性比HBrO4弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 光合作用是將光能轉化為化學能的有效途徑 | |
| B. | 氫能是一種理想的“綠色能源” | |
| C. | 煤、石油和天然氣都是可再生的化石燃料 | |
| D. | 用植物秸稈制沼氣是有效利用生物質能的方式之一 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氣溶膠的分散劑是氣體 | |
| B. | 根據分散質和分散劑的狀態,可以將膠體分為9種 | |
| C. | 氣溶膠分散質粒子直徑在1nm-100nm | |
| D. | 膠體不能透過濾紙 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaCl晶體溶于水 | B. | 氯原子結合成氯分子 | ||
| C. | 臭氧轉化為氧氣 | D. | 干冰氣化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com