
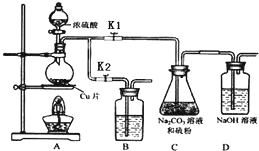
 硫代硫酸鈉(Na2S2O3)可由亞硫酸鈉和硫粉通過化合反應制得.
硫代硫酸鈉(Na2S2O3)可由亞硫酸鈉和硫粉通過化合反應制得.| 編號 | 1 | 2 | 3 |
| 溶液的體積/mL | 10.00 | 10.00 | 10.00 |
| 消耗I2標準溶液的體積/mL | 19.95 | 17.10 | 20.05 |
分析 (Ⅰ)①銅和濃硫酸加熱反應生成硫酸銅、二氧化硫和水;
②Na2S2O3在酸性溶液中不能穩定存在,二氧化硫通入碳酸鈉溶液中反應生成亞硫酸鈉和硫粉反應生成硫代硫酸鈉;裝置D是用氫氧化鈉吸收未反應的二氧化硫和產生的二氧化碳;停止C裝置反應打開K2,關閉K1;
④裝置B是利用氫氧化鈉溶液吸收多余的二氧化硫氣體;
(Ⅱ)以淀粉溶液為指示劑,用濃度為0.050mol/L I2的標準溶液進行滴定,終點現象為溶液變藍色且半分鐘內不褪色;依據反應的定量關系 2S2O32-+I2→S4O62-+2I-.計算碘單質消耗的硫代硫酸鈉,計算得到樣品中的質量分數.
解答 解:(Ⅰ)①銅和濃硫酸加熱反應生成硫酸銅、二氧化硫和水,反應的化學方程式為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
②Na2S2O3在酸性溶液中不能穩定存在,二氧化硫通入碳酸鈉溶液中反應生成亞硫酸鈉和硫粉反應生成硫代硫酸鈉,C中混合液被氣流攪動,反應一段時間后,硫粉的量逐漸減少,所以C中碳酸鈉的作用是做反應物,提供堿性環境,裝置D是用氫氧化鈉吸收未反應的二氧化硫和產生的二氧化碳,反應的離子方程式為SO2+2OH -=SO32-+H2O、CO2+2OH -=CO32-+H2O,停止C中的反應的操作是應打開K2,關閉K1 ,
故答案為:提供堿性環境,作反應物;SO2+2OH -=SO32-+H2O、CO2+2OH -=CO32-+H2O;打開K2,關閉K1;
④為防止過量的二氧化硫污染性氣體排放到空氣中污染環境,裝置B是利用氫氧化鈉溶液吸收多余的二氧化硫氣體;
故答案為:NaOH;在C中的反應停止后,吸收A中產生的多余SO2,防止空氣污染;
(Ⅱ)以淀粉溶液為指示劑,用濃度為0.050mol/L I2的標準溶液進行滴定,終點現象為溶液變藍色且半分鐘內不褪色;根據表中數據可知,第二次實驗中消耗I2標準溶液的體積偏小,舍去,則實際消耗I2標準溶液的體積的平均值是=$\frac{19.95+20.05}{2}$=20ml,則根據反應的方程式可知,2S2O32-+I2→S4O62-+2I-,所以樣品中Na2S2O3•5H2O的物質的量是0.050mol/L×0.0200L×2×10=0.02mol,則Na2S2O3•5H2O在產品中的質量分數=$\frac{0.02mol×248g/mol}{5.5g}$×100%=90.2%;
故答案為:加入最后一滴I2標準溶液后,溶液變藍,且半分鐘內顏色不改變;90.2%.
點評 本題考查了物質性質的實驗驗證和實驗方法應用,物質性質的掌握和實驗基本操作是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:解答題
 葡萄可用于釀酒.
葡萄可用于釀酒. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.| ①稱取E4.5g,升溫使其汽化,測其密度是相同條件下H2的45倍. | ①有機物E的相對分子量為90: |
| ②將此9.0gE在足量純O2充分燃燒,并使其產物依次通過堿石灰、無水硫酸銅粉末、足量石灰水,發現堿石灰增重14.2g,硫酸銅粉末沒有變藍,石灰水中有10.0g白色沉淀生成;向增重的堿石灰中加入足量鹽酸后,產生4.48L無色無味氣體(標準狀況). | ②9.0g有機物E完全燃燒時,經計算:生成CO2共為0.3 mol, 生成的H2O5.4g. 有機物E的分子式C3H6O3 |
| ③經紅外光譜測定,證實其中含有羥基,羧基,甲基; | ③E的結構簡式CH3CH(OH)COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 有機物在濾液中 | B. | 雜質在濾液中 | C. | 有機物濾紙上 | D. | 雜質在溶劑中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 溫度(絕對溫度) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
| 時間/min | CO2 | H2 | CO | H2O |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
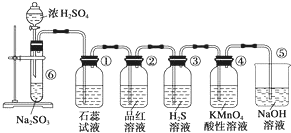 圖是實驗室制取SO2并驗證SO2的某些性質的裝置,試回答:
圖是實驗室制取SO2并驗證SO2的某些性質的裝置,試回答:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com