
分析 2Al+Fe2O3$\frac{\underline{\;高溫\;}}{\;}$2Fe+Al2O3中,Fe元素的化合價降低,Al元素的化合價升高,結合氧化還原反應基本概念及電子守恒來解答.
解答 解:(1)反應2Al+Fe2O3$\frac{\underline{\;高溫\;}}{\;}$Al2O3+2Fe中,化合價降低元素Fe所在的反應物Fe2O3是氧化劑,化合價升高元素Al所在的反應物是還原劑,化合價的升降數=轉移電子數=6,所以反應中生成2mol Fe時,轉移6mol電子,反應中生成1mol Fe時,轉移3mol電子,電子轉移情況如下: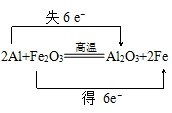 ,
,
故答案為: ;
;
(2)反應中Fe元素化合價降低,被還原,Al元素化合價升高,被氧化,Al2O3為氧化產物,
故答案為:Fe;Al2O3;
(3)由方程式可知2molAl參加反應,消耗1molFe2O3,可知氧化劑和還原劑物質的量的比1:2,
故答案為:1:2.
點評 本題考查氧化還原反應,為高考高頻考點,把握反應中元素的化合價變化為解答的關鍵,側重氧化還原反應基本概念和轉移電子的考查,題目難度不大.


 活力課時同步練習冊系列答案
活力課時同步練習冊系列答案 學業測評一課一測系列答案
學業測評一課一測系列答案科目:高中化學 來源: 題型:多選題
| A. | NH3•H2O | B. | Mg(OH)2 | C. | Na2CO3 | D. | MgCO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 自來水廠用含鐵的化合物作凈水劑 | |
| B. | 用丁達爾效應區分氫氧化鐵膠體和氯化鐵溶液 | |
| C. | 一束平行光照射蛋白質溶液時,從側面要看到光亮的通路 | |
| D. | 在三氯化鐵溶液中滴入氫氧化鈉溶液出現紅褐色沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電路中共轉移0.7mol電子 | |
| B. | 陰極得到的氣體物質的量為0.35mol | |
| C. | 陰極質量增加3.2g | |
| D. | 鋁元素以A1(OH)3的形式存在 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
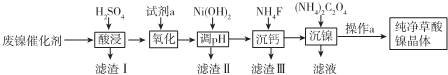
| 金屬離子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 開始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 所含碳原子數比為1:1 | B. | 體積比為1:1 | ||
| C. | 密度比為7:11 | D. | 分子數比為7:11 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
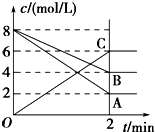 根據圖填空:
根據圖填空:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 T、W、X、Y、Z是元素周期表前四周期中的常見元素,原子序數依次增大,相關信息如下表.
T、W、X、Y、Z是元素周期表前四周期中的常見元素,原子序數依次增大,相關信息如下表.| 元素 | 相關信息 |
| T | T元素可形成自然界硬度最大的單質 |
| W | W與T同周期,核外有一個未成對電子 |
| X | X原子的第一電離能至第四電離能分別是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
| Y | 常溫常壓下,Y單質是固體,其氧化物是形成酸雨的主要物質 |
| Z | Z的一種同位素的質量數為63,中子數為34 Ni |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com