
| 實驗編號 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol•L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c( S2O82-)/mol•L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
分析 (1)平衡常數指各生成物濃度的化學計量數次冪的乘積除以各反應物濃度的化學計量數次冪的乘積所得的比值;
(2)根據方程式可知,I3-可看做I2和I-相結合形成的微粒,故發生反應的I-與被氧化的I-的物質的量比為3:2;
(3)由題目中表格數據可分析出c(I-)、c(S2O32-)濃度越大,反應速率越快,顯藍色所需時間越少,故實驗目的應是研究反應物I-與S2O82-的濃度對反應速率的影響;對比數據組①和②、數據組②和③、數據組③和④、數據組①和③,分析當其中一個變量(即一種反應物濃度)保持不變時,反應時間的變化(即反應速率的變化),然后分析當兩個變量同時變化一定的倍數時,反應時間的變化(即反應速率的變化),就可以得出其中的規律,據此計算顯色時間.
解答 解:(1)反應的平衡常數為生成物濃度的化學計量數次冪的乘積除以各反應物濃度的化學計量數次冪的乘積,則k=$\frac{c({{I}_{3}}^{-})•{c}^{2}(S{{O}_{4}}^{2-})}{{c}^{3}({I}^{-})•c({S}_{2}{{O}_{8}}^{2-})}$,
故答案為:$\frac{c({{I}_{3}}^{-})•{c}^{2}(S{{O}_{4}}^{2-})}{{c}^{3}({I}^{-})•c({S}_{2}{{O}_{8}}^{2-})}$;
(2)根據方程式可知,I3-可看做I2和I-相結合形成的微粒,故發生反應的I-與被氧化的I-的物質的量比為3:2,故答案為:3:2;
(3)由題目中表格數據可分析出c(I-)、c(S2O32-)濃度越大,反應速率越快,顯藍色所需時間越少,故實驗目的應是研究反應物I-與S2O82-的濃度對反應速率的影響;對比數據組①和②、③和④,可以看到,c (S2O82-)不變,c (I-)增大到2倍時,反應時間縮短了一半,即反應速率加快了一倍;
對比數據組②和③,可以看到,c (I-)不變,c (S2O82-)增大到2倍時,反應時間縮短了一半,即反應速率也加快了一倍;
對比數據組對比數據組①和③,可以看到,c (I-)和c (S2O82-)均增大到2倍時,反應時間為原反應時間的1/4,即反應速率加快了4倍;可見兩個反應物的濃度和反應速率之間的數學關系是:反應物濃度每增加一倍,反應時間就減少一倍,對于兩個反應物來說都是如此,
可得出結論:反應速率與反應物起始濃度乘積成正比;
對比實驗①和⑤,實驗⑤的c (I-)為實驗①的4倍,而c (S2O82-)保持不變,由此可計算實驗⑤的反應時間應為實驗①反應時間的1/4,即t1=88s×$\frac{1}{4}$=22s;
若c(I-)=0.64mol/L,c(S2O82-)=0.02mol/L,c (I-)為實驗①的16倍,而c (S2O82-)是實驗①的$\frac{1}{2}$,則顯色時間為實驗①的$\frac{1}{8}$,即11s,
故答案為:研究反應物I-與S2O82-的濃度對反應速率的影響;22;11s.
點評 本題考查化學平衡常數、氧化還原反應、影響化學反應速率的外界因素,難點是學生對圖表的觀察、分析以及學生對實驗數據的分析、整理、歸納等方面的思維能力,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4LH2O含有的分子數為1 NA | |
| B. | 常溫常壓下,1.42g Na2SO4含有的Na+離子數為0.01 NA | |
| C. | 通常狀況下,NA個CO2分子含有原子數為3 NA | |
| D. | 物質的量濃度為0.5mol/L的MgCl2溶液中,含有Cl- 個數為1 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
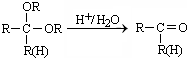
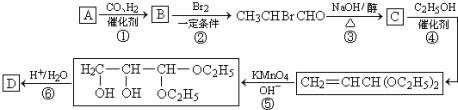
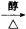 CH2=CHCHO+NaBr+H2O.
CH2=CHCHO+NaBr+H2O.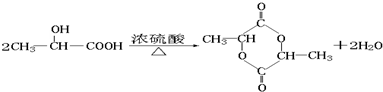 .
.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | NH4CNO和CO(NH2)2 | B. | CH2OHCHO和CH3COOH | ||
| C. | CH3OOCCH3和CH3COOCH3 | D. | 甘氨酸和CH3 CH2NO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
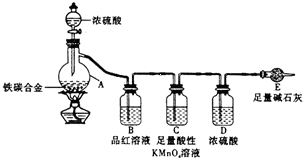 某學習小組設計了圖示實驗裝置(省略了夾持儀器)來測定某鐵碳合金中鐵的質量分數.
某學習小組設計了圖示實驗裝置(省略了夾持儀器)來測定某鐵碳合金中鐵的質量分數.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
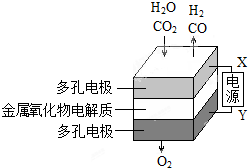 在固態金屬氧化物電解池中,高溫共電解H2O-CO2混合氣體可制備H2和CO是一種新的能源利用方式,基本原理如圖所示:
在固態金屬氧化物電解池中,高溫共電解H2O-CO2混合氣體可制備H2和CO是一種新的能源利用方式,基本原理如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | m=2x | B. | m<2x | C. | m>2x | D. | 無法判斷 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
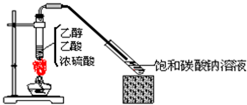 如圖所示,實驗室制乙酸乙酯1mL后,沿器壁加入紫色石蕊試液0.5mL,這時石蕊試液將存在于飽和碳酸鈉溶液層與乙酸乙酯層之間(整個過程不振蕩).對可能出現的現象,敘述正確的是
如圖所示,實驗室制乙酸乙酯1mL后,沿器壁加入紫色石蕊試液0.5mL,這時石蕊試液將存在于飽和碳酸鈉溶液層與乙酸乙酯層之間(整個過程不振蕩).對可能出現的現象,敘述正確的是| A. | 石蕊層仍為紫色,有機層無色 | |
| B. | 石蕊層有兩層,上層為紫色,下層為藍色 | |
| C. | 石蕊層為三層環,由上而下是紅、紫、藍 | |
| D. | 石蕊層為三層環,由上而下是藍、紫、紅 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AB3 | B. | AB | C. | A3B | D. | A2B3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com