
分析 設出混合氣體中CO與CO2的物質的量,根據n=$\frac{m}{M}$計算出碳、氧氣的物質的量,然后結合C、O元素守恒列式計算,然后根據M=$\frac{m}{n}$計算出混合氣體的平均摩爾質量,最后結合摩爾質量與相對分子質量之間的關系解答.
解答 解:6gC的物質的量為:$\frac{6g}{12g/mol}$=0.5mol,14g氧氣的物質的量為:$\frac{14g}{32g/mol}$=$\frac{7}{16}$mol,
設生成CO為xmol、二氧化碳ymol,
根據碳元素質量守恒可得:①x+y=0.5mol,
根據氧元素質量守恒可得:②x+2y=$\frac{7}{16}$mol×2=$\frac{7}{8}$mol,
根據①、②解得:x=0.125、y=0.375,
根據質量守恒定律可知,生成氣體的質量為4g+16g=20g,生成氣體的總物質的量為:0.125mol+0.375mol=0.5mol,
則混合氣體的平均摩爾質量為:$\frac{20g}{0.5mol}$=40g/mol,所以混合氣體的平均分子質量為40,
故答案為:40.
點評 本題考查了有關混合物反應的計算,題目難度中等,正確判斷反應物過量確定為解答關鍵,注意質量守恒在化學計算中的應用方法,試題培養了學生的化學計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | 將4gNaOH溶液溶入1L水中 | |
| B. | 常溫下,將2.24LHCl氣體溶于水配成1L溶液 | |
| C. | 含有4.9gH2SO4的溶液500mL | |
| D. | 將6.2gNa2O溶于水配成1L溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

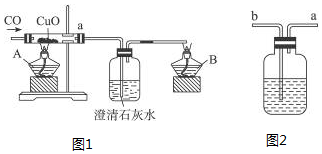
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 化學鍵 | H-H | N≡N | H-N |
| 鍵能 | 436kJ/mol | 946kJ/mol | x |
| A. | 391kJ/mol | B. | 431kJ/mol | C. | 349kJ/mol | D. | 469kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
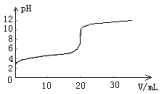 常溫下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH隨NaOH溶液體積的變化如圖所示.下列說法不正確的是( )
常溫下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH隨NaOH溶液體積的變化如圖所示.下列說法不正確的是( )| A. | 在反應過程中,c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | pH=5時,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | pH=7時,消耗NaOH溶液的體積肯定小于20.00mL | |
| D. | pH>7時,消耗NaOH溶液的體積肯定大于20.00mL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將銅插入稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| B. | 向Fe2(SO4)3溶液中加入過量鐵粉:Fe3++Fe═2Fe2+ | |
| C. | 向Al2(SO4)3溶液中加入過量氨水:Al3++3NH3﹒H2O═Al(OH)3↓+3NH4+ | |
| D. | 向Na2SiO3溶液中滴加稀鹽酸:Na2SiO3+2H+═H2SiO3↓+2Na+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ③④ | C. | ①②③ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | 用醋酸溶解CaCO3:2H+CaCO3═Ca2++H2O+CO2↑ | |
| C. | 在氯化亞鐵溶液中通入氯氣Fe2++Cl2═Fe3++2Cl- | |
| D. | NaHCO3溶液中加入過量的Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,36 g 18O2中所含的中子數為16 NA | |
| B. | 8.0 g Cu2S和CuO的混合物中含有的銅原子數為0.1 NA | |
| C. | 電解飽和食鹽水時,陽極生成22.4L氣體時,陰極生成氣體分子 NA個 | |
| D. | 標準狀況下,22.4 L Cl2與足量NaOH溶液反應,轉移電子數為2 NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com