
| A. | 用過量氨水吸收工業尾氣中的SO2:NH3•H2O+SO2═NH4++SO32-+H2O | |
| B. | MnO2與濃鹽酸反應制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| C. | 向FeBr2溶液中通入足量氯氣:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O |
分析 A.電荷不守恒;
B.氯化氫為強電解質,應拆成離子形式;
C.氯氣足量二價鐵離子、溴離子都被氧化;
D.醋酸為弱酸,應保留化學式.
解答 解:A.用過量氨水吸收工業尾氣中的SO2,離子方程式:2NH3•H2O+SO2═2NH4++SO32-+H2O,故A錯誤;
B.MnO2與濃鹽酸反應制Cl2,離子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故B錯誤;
C.向FeBr2溶液中通入足量氯氣,離子方程式:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故C正確;
D.醋酸除去水垢,離子方程式:2CH3COOH+CaCO3═Ca2++CO2↑+H2O+2CH3COO-,故D錯誤;
故選:C.
點評 本題考查離子方程式的書寫,側重考查氧化還原反應離子方程式書寫、復分解離子反應方程式書寫,熟悉物質的性質及發生反應的實質是解題關鍵,題目難度中等.


 智能訓練練測考系列答案
智能訓練練測考系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 離子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a=1,b=2 | B. | a=2,b=1 | C. | a=2,b=2 | D. | a=3,b=2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
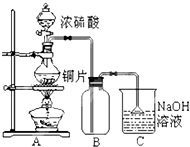 某研究性學習小組的同學為驗證濃硫酸與銅能反應而稀硫酸不能,設計了如圖所示裝置進行探究:將6.4g 銅片和含0.2moL溶質的18.4mol/L濃硫酸放在圓底燒瓶中共熱,直到無氣體生成為止.(假定在此過程溶液體積不變)
某研究性學習小組的同學為驗證濃硫酸與銅能反應而稀硫酸不能,設計了如圖所示裝置進行探究:將6.4g 銅片和含0.2moL溶質的18.4mol/L濃硫酸放在圓底燒瓶中共熱,直到無氣體生成為止.(假定在此過程溶液體積不變)| 序號 | 不合理的原因 | 誤差 (偏低或偏高) | 改變措施 |
| 方案① | 高錳酸鉀溶液中含有硫酸,與氯化鋇反應,使生成的沉淀增多 | 偏低 | 將硫酸酸化的高錳酸鉀溶液換成溴水或碘水或硝酸溶液 |
| 方案② | 不填 | 不填 | 不填 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
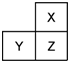 X、Y、Z是三種短周期的主族元素,在周期表中的位置如圖,X原子的最外層電子數是其次外層電子數的3倍,下列說法正確的是( )
X、Y、Z是三種短周期的主族元素,在周期表中的位置如圖,X原子的最外層電子數是其次外層電子數的3倍,下列說法正確的是( )| A. | 氣態氫化物的熱穩定性:X>Z | |
| B. | 原子半徑:X<Y<Z | |
| C. | Y和Z的最高價氧化物對應水化物均為強酸 | |
| D. | 若Z的最高正價為+m,則X的最高正價也一定為+m |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 干冰、液態氯化氫都是電解質 | |
| B. | Na2O、Fe2O3、Al2O3既屬于堿性氧化物,又屬于離子化合物 | |
| C. | 有單質參加或生成的反應不一定屬于氧化還原反應 | |
| D. | 根據是否具有丁達爾效應,將分散系分為溶液、濁液和膠體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com